Типовые факторы крови
С открытием феномена изогемагглютинации удалось доказать наличие в эритроцитах крови человека групповых и подгрупповых антигенов. Для обнаружения этих факторов потребовались специальные «реактивы» - сыворотки крови человека, седержащие соответствующие антитела. Эти групповые и подгрупповые антитела сформировались в эволюции, в связи с чем получили наименование нормальных антител. Таким образом, рабочие сыворотки, необходимые для обнаружения групповых и подгрупповых антигенов, оказались в природе в готовом виде, если можно так выразиться.
В антигенном составе эритроцитов крови человека оказались также и такие факторы, применительно к которым в сыворотке крови человека нормальные антитела не обнаруживаются. Эти так называемые дополнительные изоантигены, в дальнейшем получившие наименование типовых антигенов, обнаруживаются в эритроцитах с помощью иммунных сывороток. Сывороткц эти получаются от некоторых животных в результате их иммунизации специальными методами. Для обнаружения типовых антигенов можно пользоваться также сывороткой крови больных, иммунизированных в отношении того или иного типового фактора в результате ошибочного переливания крови, несовместимой с кровью реципиента по данному типовому фактору. Для этих целей пригодна также сыворотка крови женщин, перенесших беременность, несовместимую по типовым факторам крови матери и плода (наличие в эритроцитах крови плода антигенного фактора, отсутствующего в организме матери). В настоящее время известно уже довольно значительное количество типовых изоантигенов. Антигенная активность типовых факторов различна, в силу чего значение этих факторов применительно к практике переливания крови далеко не одинаково. Выдающийся практический интерес представляет типовой фактор, известный под названием резус-фактора.
Резус-фактор был обнаружен в эритроцитах крови человека Ландштейнером и Винером (1940) с помощью иммунной сыворотки крови кролика. Иммунизация кролика производилась эритроцитами крови мартышки (Macacus rhesus), в связи с чем обнаруженный фактор и получил название резус-фактора.
Резус-фактор обнаружен в организме человека не только в эритроцитах крови, но и в фиксированных клетках различных органов (печень, селезенка, органы пищеварительного тракта и др.), а также в незначительном количестве в жидких средах организма, в частности в плазме крови.
Резус-фактор, обнаруженный в организме человека, в отличие от резус-фактора крови человекоподобных и некоторых низших обезьян, характеризуется сложностью физико-химической структуры и высокодифференцированной иммуногенетической специфичностью.
В большинстве случаев резус-фактор у человека представляет собой комплекс антигенов.
Резус-фактор обнаруживается в эритроцитах крови человека, примерно в 85% случаев. Лица, имеющие в эритроцитах крови резус-фактор, условно обозначаются как резусположительные. Лица, у которых резус-фактор специальными методами серологического исследования не обнаруживается, условно обозначаются как резусотрицательные. При массовом обследовании такие лица составляют примерно 15%. Резус-фактор, подобно всем другим типовым факторам, распределяется у людей независимо от групповых, подгрупповых и различных типовых факторов, а также независимо от пола и возраста.
Резус-фактор является чужеродным, следовательно, иммуногенным фактором лишь для лиц, в организме которых этого фактора не имеется. В результате резус-иммунизации (переливание резуснесовместимой крови, беременность резусотрицательной женщины резусположительным плодом) у человека может возникнуть состояние резус-сенсибилизации, сопровождающееся образованием иммунных резус-антител. Нормальные, прирожденные резус-антитела, подобно групповым антителам, у человека современными методами иследования не выявляются.
Гемотрансфузионный резус-конфликт возникает у человека далеко не в каждом случае переливания резуснесовместимой крови. На 100 переливаний резуснесовместимой крови примерно лишь в 4-5 случаях клинически выявляется гемотрансфузионная реакция тон или иной силы, генетически связанная с резус-несовместимостью крови донора и реципиента. Данные эти свидетельствуют о том, что ответная реакция организма на парентеральное введение резус-антигена формируется под воздействием множества факторов, в результате чего реакция эта приобретает по существу индивидуальный характер. Возникшая у больного гемотрансфузионная резус-сенсибилизация, может оказаться весьма стойкой. Имеется наблюдения, когда резус-антитела обнаруживались в сыворотке крови больного спустя 12-15 лет после однократного переливания резуснесовмести мол крови.
Единственно надежная профилактика гемотрансфузионной резус-сенсибилизации заключается в переливании резуссовместимой крови в каждом случае переливания крови в соответствии с правилом резус-совместимости, т. е. резусположительному реципиенту (для которого резус-фактор не является чужеродным антигеном, поскольку фактор этот имеется в организме реципиента) можно переливать кровь донора как резусположительного, так и резусотрицательного, т. е. независимо от резус-принадлежности донора; реципиенцу резусотрицатпельному (для которого резус-фактор является чужеродным антигеном, поскольку его нет в организме репипиента) можно переливать только кровь резусотрицательного донора. Таким образом, для гарантийной профилактики гемотрансфузионной резус-сенсибилизации следует в каждом случае переливания крови предварительно определить резус-принадлежность реципиента и донора, как это имеет место в отношении, групповых факторов крови. Внедрение этого мероприятия в повседневную практику переливания крови пока что наталкивается на серьезные затруднения. В связи с этим действующая инструкция по профилактике осложнений, связанных с переливанием резуснесовместимой крови, предусматривает обязательное определение резус-принадлежности лишь у определенных контингентов больных, у которых возможность резус-сенсибИлизации представляется наиболее вероятной. В соответствии с указанной инструкцией по резус-фактору при переливании крови необходимо соблюдение следующих правил.
1. У каждого больного, нуждающегося в переливании крови, следует самым тщательным образом собрать анамнез о производившихся ему ранее переливаниях крови и о том, как они протекали в смысле гемотрансфузионной реакции. При наличии в гемотрансфузионном анамнезе больного указаний на частые и более или менее выраженные реакции на переливания крови необходимо исследовать кровь больного на резус-принадлежность. При резусотрицательной принадлежности больного реципиенту можно переливать только кровь резусотрицательного донора.
2. У каждой рожавшей женщины, нуждающейся в переливании крови, следует тщательным образом собрать акушерский анамнез. При наличии в акушерском анамнезе указаний на немотивированные выкидыши, внутриутробную смерть плода, заболевание плода одной из форм гемолитической болезни новорожденных (желтуха, анемия, общий отек и др.) необходимо исследовать кровь больной на резус-принадлежность и переливание крови производить в строгом соответствии с правилами резус-совместимости.
3. Обязательное определение на резус-принадлежность в связи с предстоящим переливанием крови предусматривается также и в отношении женщин-реципиентов, нуждающихся в повторных переливаниях крови (независимо от данных гемотрансфузионного и акушерского анамнеза).
4. При срочности показаний к переливанию крови, а также в случае отсутствия практической возможности определения резус-принадлежности крови больного (пп. 1-3) следует пользоваться резусотрицательной кровью впредь до установления резус-принадлежности больного, а в дальнейшем при повторных переливаниях крови придерживаться при подборе донора правила резус-совместимости. Если имеются срочные показания к переливанию крови, а резусотрицательная кровь отсутствует, то следует пользоваться предпочтительно плазмой или сывороткой крови резусположительного донора.
5. Для лечения новорожденных с признаками гемо литической болезни следует применять переливание резусотрицательной крови, несмотря на резусположительную принадлежность крови ребенка, так как в русле кровообращения ребенка циркулируют резус-антитела, выработанные организмом матери. В этих условиях переливание ребенку резусположительной крови неизбежно приведет к гемолизу перелитой крови. В силу тех же соображений кровь матери нельзя переливать ребенку, болеющему гемолитической болезнью новорожденных. К тому же кровь матери может оказаться несовместимой с кровью ребенка и по групповым факторам.
В настоящее время вся работа по исследованию крови больных-реципиентов на резус-принадлежность централизована и производится в специальных серологических лабораториях институтов и станций переливания крови. Лаборатории эти безотказно обслуживают запросы лечебных учреждений в рамках инструкции по резус-фактору. При направлении соответствующих требований в серологические лаборатории институтов и станций переливания крови следует придерживаться определенной формы сопроводительного бланка с представлением данных по следующим пунктам: 1. Наименование лечебного учреждения. 2. Фамилия, имя и отчество больного (ой). 3. Возраст. 4. Пол. 5. Группа крови реципиента. 6. Данные гемотрансфузионного анамнеза. 7. Данные акушерского анамнеза. 8. Подпись направляющего врача.
Имея в виду всемерное удовлетворение потребности лечебных учреждений в резусотрицательной крови, институты и станции переливания крови, заготовляющие консервированную кровь, в настоящее время обследуют поголовно весь свой донорский актив на резус-принадлежность. Вся консервированная кровь, заготовленнная от резусотрицательных доноров, хранится в экспедициях институтов и станций переливания крови на предмет специального назначения как дежурная кровь для резус-отрицательных больных-реципиентов. Эта кровь должна использоваться очень бережно и строго мотивированно по прямому своему назначению.
Переливание резуснесовместимой крови может привести к тяжелым последствиям, а в отдельных случаях и к смертельному исходу.
Наблюдение 3. Больной З-в, 28 лет. Болеет туберкулезом легких в течение последних 5 лет. При поступлении в больницу у больного обнаружен правосторонний фиброзно-кавернозный туберкулез легких с очаговым обсеменением в среднем поле слева. Гемоглобина 56%. Моча нормальная. В прошлом переливаний крови не имел. Спустя 2 месяца после госпитализации под местной анестезией произведена нижнезадняя торакопластика справа. После операции перелита одногруппная [0(I)] свежекоьсервнрованная кровь в количестве 175 мл. Переливание крови проведено без какой-либо клинически выраженной побочной реакции. В моче, исследованной спустя 2 дня после переливания крови, были обнаружены существенные изменения: белка 3,3‰, лейкоцитов 1-3 в поле зрения, цилиндров гиалиновых 0-3 в поле зрения, зернистых 1-2 в редких полях зрения, почечного эпителия до 2 в редких полях зрения, плоского в умеренном количестве, слизь в порядочном количестве. При ближайшем исследовании мочи спустя 4 дня и в дальнейшем, вплоть до второго переливания крови, никаких уклонений от нормы в моче уже не было обнаружено.
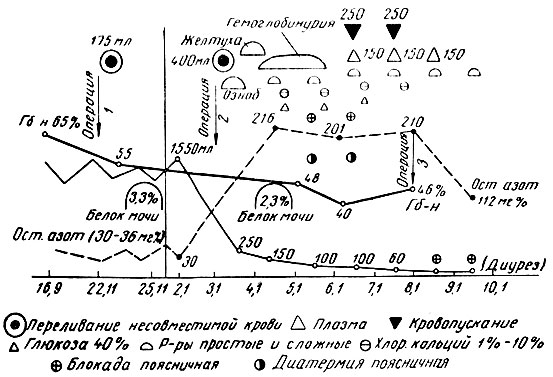
Диаграмма 2. Наблюдение 3. Больной З-в, 28 лет. Фиброзно-кавернозный туберкулез легких. Двукратное переливание резуснесовместимой крови. Гемолитическая реакция. Смертельный исход
Спустя 42 дня после первой операции под местной анестезией произведена передневерхпяя торакопластика справа. По окончании операции переливание одногруппной [0(I)] крови в количестве 400 мл от двух доноров без какой-либо побочной реакции во время переливания крови. Спустя 11/2 часа после переливания крови - потрясающий озноб в течение часа, головная боль. После обогревания и горячего питья общее состояние больного улучшилось и в течение ближайших нескольких часов оставалось удов, летворительным. Однако к утру состояние больного резко ухудшилось: упала сердечная деятельность, пульс частый, очень слабого наполнения, дыхание затрудненное, синюшность покровов с желтушным оттенком, рвота, головная боль. Во вторую половину дня больной самостоятельно помочился. Моча в количестве 150 мл коричневато-красного цвета. Данные анализа: удельный вес 1017, белка 2,3‰, желчные пигменты не обнаружены, уробилин в норме, реакция на кровь резко положительная, в осадке лейкоцитов 2-3 в поле зрения, эритроциты свежие 1-2-3 в поле зрения, цилиндры гиалиновые 1-2-3 в поле зрения, зернистые 0-1 в поле зрения, восковидныо 2-3 в поле зрения, почечный эпителий 1-3-4 в поле зрения, плоский - в небольшом количестве, кровяной детрит в большом количестве. В этот день остаточный азот крови достиг 216 мг%, билирубин крови 0,25 мг% по ван ден Бергу. В последующие дни диурез упал до 100-60 мл в сутки.
В связи с выявлением гемолитической реакции были проведены следующие лечебные мероприятия: двусторонняя поясничная новокаиновая блокада, диатермия поясничной области, кровоизвлечение в количестве 250 мл с последующим замещением плазмой, обильное парентеральное введение жидкостей, промывание желудка, хлористый кальций внутривенно как диуретическое средство. Все эти мероприятия проводились повторно, однако без заметного эффекта, и на 5-е сутки после второго переливания крови, осложнившегося гемолитической реакцией, наступила анурия.
Состояние больного к этому моменту резко ухудшилось. Больной жалуется на крайнюю слабость, мучительную головную боль. Покровы и видимые слизистые бледны, с оттенком желтушности. Язык суховат. Пульс 60 ударов в минуту, ритмичный, несколько напряженный; дыхание поверхностное, замедленное; кровяное давление 140/90 мм ртутного столба; частая рвота. Состояние ареактивности, адинамии. Остаточный азот крови 210 мг%.
Ввиду безэффективности проведенной терапии и нарастающей интоксикации, после консультации с урологом на 6-е сутки после второго переливания крови произведена декапсуляция обеих почек под местной инфильтрационной новокаиновой анестезией. Фиброзная капсула с обеих сторон очень дряблая, легко рвется, а потому удалена частями. К декапсулированным почкам подведены тампоны. Кетгутовые швы на мышцы в два ряда, швы на кожу, сухая асептическая повязка.
Произведенная операция не дала эффекта. Моча не появилась. Состояние больного продолжало ухудшаться с каждым часом, и к исходу 7-х суток после второго переливания крови, осложнившегося гемолитической реакцией, при явлениях нарастающей интоксикации больной скончался. Произведенное в связи с гемолитической реакцией серологическое исследование крови больного подтвердило принадлежность больного к группе 0(I). По типовым свойствам кровь больного оказалась резусотрицательной. В сыворотке крови больного обнаружены были резус-антитела с титром 1:8. Все три донора, кровь которых была перелита в этом случае, оказались при исследовании резусположительными.
Анатомический диагноз. Фиброзно-кавернозный туберкулез верхней доли правого легкого. Творожистый некроз лимфатических узлов ворот левого легкого. Полная облитерация плевральных полостей. Состояние после операции торакопластики. Внутрисосудистый посттрансфузионный гемолиз крови. Выделительный нефроз. Свежая операция частичной декапсуляции почек. Мнение прозектора. Смерть больного наступила от острого нефрозо-нефрита на почве переливания несовместимой крови.
В данном случае имело место двукратное переливание одногруппной резуснесовместимой крови в количестве 175 мл и 400 мл с бурно развившейся гемолитической реакцией на второе переливание крови, произведенное спустя 42 дня после первого переливания. Больной в прошлом переливаний крови не имел; следовательно, не было и условий для резус-иммунизации больного в прошлом, до поступления его в больницу. Между тем уже з результате двух переливаний резуснесовместимой крови больной выработал резус-антитела с довольно высоким титром (1:8). Характер реакции больного на второе переливание крови (бурно протекшая гемолитическая реакция с массивным внутрисосудистый гемолизом) дает некоторые основания предположить, что больной выработал иммунологическую реакцию с образованием антител уже в ответ на первое переливание резуснесовместимой крови в количестве 175 мл. Таким образом, в данном случае мы встретились с иммунологической реакцией, протекшей с необычной для резус-фактора активностью. Следует, однако, отметить, что природа основного заболевания больного (туберкулез легких), по-видимому, не определила собой в данном случае особенностей и исхода гемолитической реакции, Так как в нашем опыте зарегистированы случаи многократных переливаний резуснесовместимой крови при туберкулезе без какой-либо побочной реакции со стороны больных.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'