Индивидуальность - это здоровье. Индивидуальность - это болезнь

Индивидуальность - это здоровье. Индивидуальность - это болезнь
Всякое человеческое познание начинается с созерцаний, переходит от них к понятиям и заканчивается идеями.
Среди тысяч людей сотни совместимы по антигенам эритроцитов (группам крови). Среди миллионов людей никто не совместим по антигенам лейкоцитов (групп тканей нет). Генетический алфавит. Связь букв этого алфавита с болезнями. Клеточные органы чувств - рецепторы. "Покажи мне свой рецептор, и я скажу, чей ты". Одноглазый Циклоп или двуединый Кентавр?
Что же это за таинственная индивидуальность, так зримо отличающая один организм от другого и в то же время связанная не с психическими свойствами или поведенческими реакциями, а с микроструктурами клеточного царства?
Каждому хорошо известно, что у разных людей неодинаковые группы крови, но все же людей со сходными группами крови подобрать совсем несложно. Однако и эта знакомая даже школьникам истина была не столь уж очевидной еще сто лет назад. Только в 1901 г. 34-летний ассистент Венского университета Карл Ландштейнер показал, что красные кровяные тельца - эритроциты в жидкой части крови - плазме других людей могут в отдельных случаях склеиваться в более или менее крупные сгустки - агглютинаты. Два антигена, обозначенные Ландштейнером заглавными буквами латинского алфавита A и B, и два вида антител к ним - анти-A и анти-B и определяют основные группы крови: A, B и AB. Несколько позже, в 1907 г. чешский врач Ян Янский открыл и четвертую группу крови, эритроциты которой не содержат антигенов А и В, но сыворотка склеивает эритроциты всех других групп крови (впоследствии эту группу стали называть первой). Чисто теоретические выкладки Ландштейнера были не сразу поняты практическими врачами, но в 1909 г. американец Р. Оттенберг предложил капельные пробы сочетаний плазмы крови с разными эритроцитами (или наоборот) считать показателем совместимости при переливаниях крови в клинике. Разразившаяся вскоре первая мировая война - эта травматологическая кровопролитная эпидемия апробировала и утвердила метод переливания крови в тысячах госпиталей.
В последующие годы ученые открыли еще ряд антигенов, присущих эритроцитам одних групп людей и отсутствующих в эритроцитах других (они так и стали называться - групповыми факторами), но эти факторы не оказывали сколько-нибудь важного влияния на исходы переливаний крови. Главные антигены эритроцитов, входящие в систему АВО, вполне могут быть обозначены как антигены совместимости крови, но их истинное биологическое значение пока не совсем ясно.
Основная задача эритроцитов - это доставка кислорода из легких во все ткани организма. Чтобы осуществить напряженную транспортную функцию, эритроцитам нужно связать как можно больше кислорода, поэтому даже ядро эритроциту помеха. Один эритроцит содержит несколько миллиардов молекул гемоглобина, белкового пигмента красного цвета. В состав гемоглобина входят молекулы железа и хрома. Хром расщепляет молекулярный кислород воздуха на атомарный (т. е. переводит O2 в два O), а железо образует с ним непрочный химический комплекс, чтобы потом легко отдать кислород тканям. Под электронным микроскопом эритроциты похожи на резиновые мячики, сдавленные с двух сторон. Такая форма двояковогнутых дисков обеспечивается специальным каркасом, состоящим из особых белков (спектрцнов) и призванным сообщить эритроцитам - этим контейнерам гемоглобина надежность и долговечность. В решетке из спектринов, противостоящей деформациям, размещены углеводно-белковые комплексы, которые могут отщепляться от поверхности эритроцитов и попадать в окружающие жидкости. К числу их и относятся антигены А и В, которые определяются на поверхности эритроцитов и в жидкостях организма.
* * *
Следующий шаг к изучению анатомических субстратов индивидуальности был сделан почти через 40 лет, когда от переливаний крови медицина перешла к следующему этапу замены живого - пересадке тканей. Оказалось, что переливание безъядерных эритроцитов не может быть даже отдаленно сравнимо с трудностями приживления массы ядросодержащих клеток, входящих в состав кожи или внутренних органов. Сразу после второй мировой войны, которая к многочисленным травматическим увечьям прибавила еще и печально частые обширные ожоги тела, хирурги все больше начали применять метод пересадки донорской кожи для закрытия раневой поверхности. Собственная кожа больного, перемещенная из одного участка тела на другой, приживала навечно. Но кожа, полученная для пересадки даже от близкого родственника, бесследно рассасывалась или отторгалась в виде сухой корки уже через две-три недели после операции. Естественно, что врачи старались при пересадках соблюсти все принципы, изученные на примерах переливания крови, но законы жидких тканей никак нельзя было применить к тайнам совместимости ядерных клеток.
В середине 60-х годов группа исследователей, руководимая французским биологом Жаном Доссе, сообщила о том, что ими обнаружен ряд антигенов, присущих ядросодержащим клеткам крови - лейкоцитам. Их было уже не два, как у эритроцитов, а десять, поэтому подбор людей, сходных по этим белкам (а их у каждого человека несколько, и комбинация их весьма прихотлива) представлялся крайне проблематичным.
Уже в первых публикациях было установлено два очень важных обстоятельства. Первое состояло в том, что вновь открытые антигены были присущи не только лейкоцитам, но и всем иным ядросодержащим клеткам организма. Иначе, были открыты антигены, играющие ключевую роль в явлениях совместимости всех тканей и органов, поэтому справедливо названные трансплантационными. Новая система антигенов тканевой совместимости, впервые выявленная при лабораторном анализе лейкоцитов крови, получила в специальной литературе сокращенное обозначение HLA (от первых букв англ. Human Leucocyte Antigens), а отдельные ее составляющие антигены стали обозначать цифрами 1, 2, 3 и т. д.
Второе важное наблюдение состояло в том, что распределение HLA-антигенов оказалось разным у представителей разных рас и национальностей. Первым на это обратил внимание все тот же Ж. Доссе, когда к своему удивлению обнаружил, что антигены, изученные у французов, встречаются у японцев совсем в другой комбинации. С 1966 г. интенсивное исследование структуры антигенов тканевой совместимости по инициативе Всемирной организации здравоохранения стало проводиться во всех странах мира. Вскоре карта мира оказалась покрытой иммунологическими иероглифами, показывающими, где и в каком сочетании встречаются антигены HLA. И вот тогда оказалось, что цепочки этих антигенов у представителей европейских стран отличны от таковых у монголоидов, а у жителей Галапагосских островов или эскимосов Аляски есть свои давние генетические особенности. Очень распространенные в Европе и Америке антигены под номерами 1 и 2 реже встречались у жителей стран Азии, которые чаще содержали антигены 9 и 11, а у представителей негроидной популяции существует своя частота таких же показателей.
Теперь, пожалуй, нет необходимости подобно Туру Хейердалу снаряжать экспедицию на тростниковой лодке, чтобы доказать миграцию населения из Южной Америки на острова Полинезии. Достаточно взглянуть в современный атлас распространения HLA-антигенов и с уверенностью сказать, что в обоих этих географических регионах есть общие генетические маркеры. Правда, возможности преодоления древними перуанцами огромных расстояний с помощью плотов из бальсовых бревен иммунологи доказать не могут, это прерогатив мужественных путешественников Хейердалова племени.
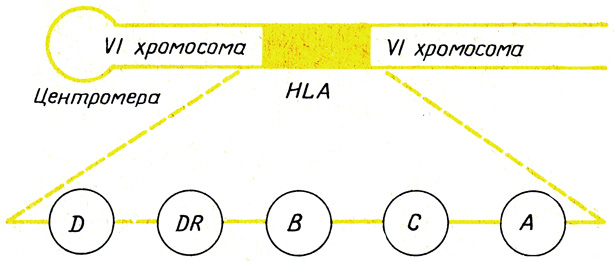
Рис. 13. Схема расположения генетических локусов HLA на VI хромосоме человека, определяющих антигены тканевой совместимости
Но вернемся к биологическим проблемам. Сегодня нам известно, что антигены тканевой совместимости, определяющие индивидуально-биологические свойства человеческого организма, контролируются определенным участком VI хромосомы человека. Этот участок включает в себя пять сегментов, их называют генетическими локусами. После нескольких рабочих совещаний специалисты решили дать этим локусам международную номенклатуру, назвав каждый из них буквами латинского алфавита. В локус А входит 20 известных сегодня антигенов, в локус В - 40, в локус С - 8, в локус D - 12 и в локус DR - 10 антигенов (рис. 13). Вот в какую сложную схему за неполных 30 лет изучения этого вопроса разрослась карта генетических маркеров человеческой индивидуальности; к 1980 г. обнаружено немногим меньше 100 составных факторов, определяющих прихотливый узор организмов рода человеческого. Еще совсем недавно казалось несправедливым, что среди исследователей эритроцитарных антигенов есть Нобелевский лауреат - Карл Ландштейнер - первооткрыватель групп крови, а среди испытателей столь сложной HLA-системы такового не было. Но в 1980 г. Нобелевский комитет исправил эту несправедливость, присудив свою премию по разделу медицины пионеру данной проблемы - французскому профессору Ж. Доссе.
Когда в 1965 г. стало известно о существовании десяти тканевых антигенов, казалось, что выбор донора для практической пересадки непомерно труден. Им теоретически мог стать лишь один из 500 обследованных. Позже, в начале 70-х годов, когда число выявленных антигенов возросло до 30, иммунологи развели руками: для реального подбора необходмо изучить 5000 человек. А сегодня!..
Нетрудно подсчитать, что количество возможных сочетаний из уже известных антигенов тканевой совместимости во много раз превосходит число людей, одновременно живущих сегодня на нашей планете. Больше того, возможно, что и в далекой истории ни у кого из нас не было прототипа, антигены которого сошлись бы с нашими, как хитроумно расположенные узоры отпечатков пальцев. Природа создала такое разнообразие белковых кирпичиков индивидуальности всего тела, преследуя главную задачу: чем более разнообразен состав генетического алфавита данного биологического вида, тем лучше он приспособлен к выживанию и противодействию вредным влияниям внешней среды, тем он биологически устойчивей. Мы не зря здесь применили сравнение с генетическим алфавитом, так как чем больше букв входит в состав алфавита, тем большее количество слов можно из них составить и тем легче выразить все оттенки умозаключений. Из обширного арсенала антигенов тканевой совместимости эволюция свободно формирует необозримое разнообразие генетических комбинаций, иначе говоря, генотипов, носителем одного и неповторимого, из которых является каждый из нас.
* * *
Ну а практические задачи пересадки органов и тканей? Казалось бы, дело здесь обстоит безнадёжно, ведь полное генетическое сходство возможно лишь между однояйцевыми близнецами (организмами, развившимися из одной яйцеклетки), а все остальные даже близкие кровные родственники - несовместимые индивиды. Это действительно так, но всё же упорное стремление медиков поставить иммуногенетику на службу самой дерзновенной области хирургии - замене больных или поврежденных органов - принесло свои плоды.
Мы уже говорили, что все антигены тканевой совместимости находятся под контролем пяти точечных участков - локусов шестой по счету хромосомы человека. Поскольку в ядре каждой клетки нашего тела парный набор хромосом, то и представители каждого из пяти локусов представлены парой, итого у каждого из нас десять генетических символов индивидуальности. Но сравним три слова:
МАТЕМАТИКА
БАЛЛИСТИКА
ЗНАХАРСТВО
Что общего и разного в этих словах? Между первым и вторым словами пять различий по буквам, между первым и третьим словами их семь. Кроме того, по расположению букв конец первого и второго слова совпадают, а у первого и третьего такого группового совпадения букв нет. Можно с уверенностью сказать, что хотя каждое из приведенных слов означает совсем несхожее понятие, но составные части алфавита в первых двух словах более близкие. Поэтому, если перевести эту игру слов на язык антигенов тканевой совместимости, то между первым и вторым словом имеется большая общность, чем между первым (а также вторым) и третьим. Следовательно, успех при пересадке органа у индивидов с более близким составом антигенов (а особенно, если совпадают блоки букв, как говорят биологи, гаплотипы) значительно более вероятен. Поскольку при пересадке органов больным проводится специальный курс лечения, подавляющий иммунитет, то реакцию отторжения ткани донора при его специальном антигенном подборе подавить легче, чем при полном генетическом несходстве. Статистика исходов операций по пересаде почки и сердца во всех клиниках мира свидетельствует о верности такого подхода.
Строго говоря, указанные выше три слова мы должны были бы обозначить не буквами, а цифрами, ну хотя бы порядковыми номерами букв алфавита. Уместность такого шифра объясняется тем, что, как это было указано выше, антигены HLA принято обозначать не буквами, а цифрами. Тогда бы слово "математика" выглядело такой колонкой цифр - 13, 1, 19, 6, 13, 1, 19, 10, 11, 1; слово "баллистика" - 2, 1, 12, 12, 10, 18, 19, 10, 11, 1; а слово "знахарство" - 9, 14, 1, 22, 1, 17, 18, 19, 3, 15. Но и это приближение страдало бы существенной неточностью: в генетическом коде антигены тканевой совместимости не повторяются, одна и та же цифра не встречается у одного человека дважды. Исключение составляют лишь нечастые случаи, когда у отца и матери был одинаковый антиген тканевой совместимости, который их ребёнок унаследовал в двойном количестве, т. е. у него имеется какой-то одинаковый крохотный участок на обеих шестых хромосомах. В таком случае в слове из десяти букв одна буква повторялась бы дважды и обе они обязательно при этом стояли бы рядом. Ну например, как в слове "расстояние", где цифровой порядок букв был бы таким - 17, 1, 18, 18, 19, 15, 32, 14, 10, 6.
Такие совпадения по общему для родителей генетическому признаку биологи называют гомозиготой (от греч. "Homo" - общий, одинаковый и "Zygota" - спаренная, так называют обычно оплодотворенную яйцеклетку). Совпадения по антигенам тканевой совместимости, иначе HLA-гомозиготы, встречаются нечасто. Но иммунологи обратили внимание на то, что такие люди чаще болеют... раком! Казалось бы, какая далекая связь! Антигены тканевой совместимости - маркеры индивидуальности, изучение которых было стимулировано запросами восстановительной хирургии, и зловещее заболевание. Но тщательно исследуя эту связь, специалисты пришли к весьма далеко идущим выводам.
* * *
В науке часто возникает парадоксальная ситуация, когда по дороге к намеченной цели луч знания освещает другой неясный вопрос, который оказывается в дальнейшем столбовой дорогой. Иное направление, ответвившееся от первоначально принятого, становится ещё более обещающим и плодоносным, а изначальное усилие по прихоти всемогущего случая приводит к совершенно непредвиденным последствиям.
Мог ли знать скромный врач Роберт Майер, случайно отметивший в бытность свою на острове Ява, что венозная кровь у туземцев светлее, нежели у европейцев, что этот незначительный факт приведет к открытию закона сохранения энергии? Лёгкое подергивание отрезанной лягушачьей лапки, подмеченное Гальвани, дало начало всему тому разделу науки, который обогатил нас электростанциями и многоголосым эфиром. А к чему привёл известный эпизод, когда завернутая в светонепроницаемую бумагу фотографическая пластинка была случайно оставлена рядом с куском урановой смоляной руды и потемнела, несмотря на защитное покрытие? Привело это ни мало ни много к открытию радиоактивности, а потом и к рождению новой технической эры...
Мы уже знаем, что побудительной причиной анализа тканевых антигенов явилась потребность выбора наиболее подходящего донора для целей трансплантации органов. В онкологической клинике в парижском предместье Вильжуиф молодой врач Амиель изучал этот вопрос применительно к пересадке костного мозга, которая подчас является единственной мерой помощи больным с злокачественным поражением кроветворной ткани. Подбирая наиболее совместимого донора костного мозга, Амиель обратил внимание на то, что у здоровых людей и больных лейкозами имеется различие в частоте встречаемости отдельных HLA-антигенов. Публикация этой работы в 1967 г. дала новый импульс иммунологическим исследованиям: антигены индивидуальности могут быть связаны с болезнями. Параллельно с открытием все новых показателей генетической индивидуальности началась интенсивная работа по проверке этих показателей у здоровых людей и больных различными заболеваниями. Несмотря на сотни статей в специальных журналах, эту работу по изысканию индивидуальной предрасположенности человека к болезненным реакциям сейчас можно считать лишь прологом к будущим открытиям.
Уже сейчас иммунологами накоплено огромное количество сведений о состоянии антигенов тканевой совместимости у людей при самых разнообразных заболеваниях. Пасьянсы раскладываются не на ломберных столиках, а в электронной памяти счетных машин. Позитивные связи, негативные связи, степени риска, взаимосочетания антигенов - вот когда иммунология, кажется, стала соответствовать постулату Иммануила Канта о том, что "в естественных науках, в собственном смысле слова, ровно столько науки, сколько в них содержится математики".
Оказалось, что целый ряд заболеваний может быть лучше диагностирован по анализам крови (имеется в виду изучение антигенов HLA), чем по сумме всех других болезненных отклонений. Так, например, при заболевании суставов позвоночника - анкилозирующем спондилите почти у всех больных имеется антиген с порядковым номером 27, а у здоровых он обнаруживается крайне редко. При кожном заболевании псориазе очень часто встречается сочетание антигенов 13 и 17, при ревматоидном артрите - антигены 3 и 40, при некоторых заболеваниях печени - антиген 8, при рассеянном склерозе - антигены 3 и 7, при сахарном диабете - антигены 15 и 18. Здесь мы указали лишь очевидные связи, когда врачи говорят о высоком риске заболеть определенным заболеванием человеку с данным генотипом HLA-антигенов. Но многие возможные ассоциации еще только исследуются.
Интересно, что были обнаружены не только позитивные, но и негативные связи болезней с антигенами тканевой совместимости, когда у людей с данным антигеном такое-то заболевание почти не встречается. Оказалось, что пациенты с анкилозирующим спондилитом почти никогда не страдают острым аппендицитом (связь по антигену 27), крайне редко сочетаются псориаз с хроническим гепатитом (антиген 1) или системной красной волчанкой (антиген 8), а диабет редко сопутствует множественному склерозу (антиген 7). Столь чудесное и давно лелеемое медициной выяснение связи индивидуальной конституции и нездоровья привело к современному пониманию того, что существует, по-видимому, две категории генов иммунологической индивидуальности: одни из них делают нас чувствительными к данному заболеванию (гены-провокаторы), а другие, наоборот, устойчивыми к этому страданию (гены-протекторы, или защитники).
Гуманной идеей отечественной медицины, которую всегда проповедовали лучшие ее представители - Г. А. Захарьин, С. П. Боткин, Н. А. Семашко и другие, было профилактическое направление, в основе которого лежало стремление не лечить, а предупредить болезнь. Материалистическое представление о факторах биологической индивидуальности и выявление их связи с патологией человека являются конкретной предпосылкой для скорых побед медицинской реабилитации. Знание антигенного спектра тканей человека позволит с учетом всех изученных степеней риска исключить или по крайней мере ослабить в каждом отдельном случае реальную угрозу и проводить направленное медицинское обследование населения.
Объяснить механизмы связей болезней с антигенами человека пока трудно. Известно, что отдельные факторы, из которых соткана индивидуальность человека, присущи и простейшим организмам - микробам. Только если генетический код человека напоминает, как уже говорилось, сложное слово, то код микроба - буква. А если данная буква входит в состав слова, определяющего конституцию человека? Тогда такой индивид не будет вырабатывать иммунитет против данного микроба, так как последний не окажется для него в полной мере чужеродным. Формы паразитирования в природе многообразны, и возможно, инфекционные болезни являются во многом формой индивидуально приспособленного микробного иждивенчества. Но это может быть отнесено к таким заболеваниям, которые являются очевидно или условно инфекционными (туберкулез, ревматизм, бронхиальная астма), а как быть с заболеваниями, в возникновении которых микробам видной роли не принадлежит, а от состава HLA-антигенов определенная зависимость просматривается (шизофрения, диабет, нарушения скелета)? Для того чтобы понять тонкие причины столь уникальных свойств клеток человеческого организма, ученым пришлось самым кропотливым образом препаровать саму клетку и особо внимательно ее внешнюю оболочку - клеточную мембрану.
* * *
Наружная клеточная мембрана является не только пограничной оболочкой, отгораживающей внутриклеточное царство от внеклеточной галактики, она служит еще и тончайшим приемным устройством для многочисленных внешних сигналов и инструментом для межклеточных контактов. Известный американский биолог Г. Никольсон писал: "Поверхность клеток - важнейшее место контроля их роста, деления, развития, связей, дифференцировок, смерти". Мало того что клеточная (или, как еще ее называют, плазматическая) мембрана избирательно регулирует поступление разных веществ внутрь клетки. При этом клеточные мембраны являются не пассивным фильтром, а живой организацией, способной к поразительным процессам: например, мембраны способствуют иногда активному переносу веществ из растворов с меньшей концентрацией в растворы с более высокой концентрацией(!). Здесь также находятся многочисленные рецепторы, справедливо называемые "органами чувств" клетки.
50 лет назад американские биологи Гортер и Грендел высказали предположение, что клеточная мембрана состоит из слоя липидов и белков ("сандвич"), позже электронная микроскопия подтвердила такое слоистое строение оболочки. Поэтому внутрь клетки легче попадают вещества, растворимые в липидах. Свободное передвижение молекул белка вдоль по плазматической мембране способствует экстренной сборке рецепторов - специализированных участков для получения и переработки, а также выведения разнообразной информации.
Клеточные рецепторы имеют сложное строение, они состоят из различных сахаров и белков. Сахара играют роль решетки, в которой застревают и крепятся белковые молекулы. Свободно передвигающиеся белки, поступающие из внутриклеточных резервуаров, задерживаются сахаристыми ветвями рецепторного каркаса, которые и удерживают их в определенном положении наподобие якоря, удерживающего судно в море. Определенное сочетание белков обеспечивает особенности, или, как говорят, специфичность, рецепторов. Клетка получает множество самых разнообразных сигналов и взаимодействует с другими клетками. Для каждого вида молекул-гормонов, витаминов, вирусов или бактерий есть свой тип рецептора. Поэтому инженерная деятельность сахаров, постоянно конструирующих на клеточной мембране соответствующие воспринимающие приборы, есть работа чрезвычайной важности.
Тонкий механизм действия рецепторов лучше изучен на примерах взаимодействия с гормонами. Каждый гормон, в какой бы железе внутренней секреции он ни вырабатывался, попадает в кровь, а оттуда поступает в клетки, имеющие к нему чувствительные рецепторы. Несмотря на чрезвычайно низкую концентрацию некоторых гормонов в крови (10-7 - 10-8 моля), действие их на чувствительную клетку обнаруживается уже через несколько секунд после выработки. А много ли на клетке рецепторов к гормону? Подсчитано, что в клетке печени на мембране содержится более 100000 рецепторов к глюкагену и 250000 рецепторов к инсулину. После того как гормон связался с рецептором, они образуют комплекс, который может изменить проницаемость мембраны или ход внутриклеточных биохимических реакций. Следствием этого является синтез клеткой тех или иных биологически активных соединений, в том числе и нового гормона. Возможно, что под действием данного гормона повысится (растормозится) чувствительность клетки к гормону иного порядка.
Помимо рецепторов к гормонам на наружной поверхности клетки, существуют таковые и внутри ее, их называют цитоплазматическими. Но они не плавают в содержимом клетки - цитоплазме, а крепятся на внутренних мембранах. Наружный рецептор может передавать сигнал внутреннему или просто открывает доступ гормону к внутреннему рецептору. Сочетание рецептора с молекулой гормона, прочное, как штепселя с розеткой, адресуется непосредственно в верховный штаб клетки - ее ядро. Воспринимающий участок ядерной ДНК, называемый акцептором, под действием этого комплекса меняет характер центральных клеточных команд.
Мы так подробно остановились на строении гормональных рецепторов потому, что принцип их действия, как и связь "черты* внешнего "лица" клетки с ее внутренним ядром, присущ всем другим рецепторам. На всех соматических клетках, а их в организме великое множество - 1014, независимо от их физиологического назначения, существуют и маркеры индивидуальности - антигены тканевой совместимости. Они входят составной частью, как кирпичики, в сооружение рецепторов любого назначения. Независимо от того, улавливает ли данный рецептор нервный импульс или гормональный сигнал, у него есть своя эмблема причастности к данному организму, это залог кооперативной, совместной деятельности всех клеток единого тела.
В принципе улавливать гормональный сигнал может любой чувствительный к нему рецептор (на этом построены некоторые виды лечения, когда вводится гормон, посторонний организму). Но сотрудничать с другими подобными клетками и обмениваться физиологическими сигналами будут лишь те, которые имеют аналогичные "визитные карточки". Так, принять и обработать мяч может игрок в любой спортивной форме, но содружественный план игры будут выполнять лишь участники одной команды. А если в эту команду попадет "лазутчик* из другого спортивного общества или данный игрок теряет спортивную форму, то игра расстраивается. Так изменение в соотношении некоторых гормональных рецепторов (например, поломка HLA-молекул) или их искажение (например, имитация HLA-молекулами рецептора к гормону) может стать причиной эндокринного заболевания. Это один из возможных путей объяснения связи заболеваний с HLA-антигенами.
В отличие от всех других клеток организма лимфоциты несут на своей мембране рецепторы, распознающие HLA-молекулы других клеток. Именно благодаря наличию таких проверяющих устройств лимфоциты и осуществляют дозорные функции в организме. А этих лимфоидных "сыщиков" в организме много - 1012, и 70% из них Т-клетки. Мы уже указывали, что число рецепторов к гормону на поверхности соматической клетки очень велико. Но сколько же HLA-рецепторов у Т-лимфоцитов? Если принять, что собственных генетических букв в алфавите данного организма не более 10, а изменена может быть любая из них или их сочетание, то простой математический подсчет показывает, что лимфоцит должен нести не менее 103 - 104 рецепторов. А если это так, то на мембране Т-клетки почти не остается места для иных нетрансплантационных антигенов (т. е. не связанных с антигенами тканевой совместимости). Не следует забывать, что у Т-клетки есть еще и иные рецепторы (к гормонам, нервным импульсам).
Из этого можно заключить, что все внешние агенты - бактерии, вирусы, химические агенты, растворимые чужие белки, попадая в организм, связываются с его антигенами и только после этого распознаются соответствующими рецепторами Т-клеток как чужеродные. Эти "измененные свои" антигены служат мишенью для возникающих цепных иммунных реакций. Такая теория "самораспознавания", недавно появившаяся в иммунологии, пока не является общепринятой, но математически она доказывается логичнее. Остается неясным, имеет ли Т-лимфоцит один рецептор к HLA-антигенам или это двойной рецептор с усиком к "своему" и другим усиком к "чужому".
Помимо такого сложного органа чувств, существуют рецепторы, характерные для Т-клеток и присущие Б-лимфоцитам (последние всегда иммуноглобулины). Отличительные особенности таких рецепторов иммунологи используют для лабораторной оценки состояния и количества Т- и Б-лимфоцитов. Наконец, имеются рецепторы третьего порядка, которые контролируются генами, определяющими способность данного организма отвечать на один антиген сильно, а на другой - слабо. От этих последних генов силы иммунного ответа связь с болезнями зависит весьма конкретно.
Все антигены тканевой совместимости, принимающие участие в построении рецепторов лимфоцитов, выведены на мембрану клетки, как клавиши рояля. Сам же набор создания специфической мелодии связан с внутриядерными хромосомами, а точнее, их участками локусами, о которых уже было много сказано. Антигены являются сигналами функционирующих генов, выведенными на клеточную оболочку, а их раздражение соответственно перестраивает работу отдельных генов, которые в конечном счете обеспечивают кооперацию различных клеток и всю сложную цепную реакцию иммуногенеза. Постоянная игра "ген - антиген - ген" происходит опять-таки с участием прямых и обратных отрицательных связей, кадс взаимодействие штаба с периферическими подразделениями.
Если клетка теряет свои антигены тканевой совместимости, а это может быть как в экстремальных условиях, так и в обычных, физиологических, то через короткий срок они опять возобновляются. Это является следствием генного контроля антигенного представительства. Нарушение или искажение этого четко выверенного механизма приводит к появлению клетки, а потом, возможно, и клеточной массы, не подобной клеткам организма. Так возникает опухоль.
* * *
В конце этой главы нам хотелось затронуть ряд внеиммунологических казусов. А может статься, что не так уж далеки они от нашей темы.
Изучение антигенов тканевой совместимости в каждом случае требует многочасового труда сотрудников хорошо оснащенной лаборатории. Но вот в 1976 г. журнал "Science Digest" сообщил, что собак научили по запаху находить людей с совместимыми тканевыми антигенами (т. 80, № 5, с. 17).
Ниже будет сказано, что размножение млекопитающих происходит с инстинктивным отбором особей, несовместимых по трансплантационным антигенам. Но что в этом случае руководит животными? Известно, что поведенческие реакции у животных - от простейших до высших - во многом определяются феромонами - пахучими веществами, выделяемыми железами во внешнюю среду. В природе феромоны (именно они, а не внешний вид животного) помогают партнерам найти друг друга для продолжения рода, препятствуя при этом невыгодному скрещиванию между близкими видами.
В эксперименте американские исследователи установили, что при смешивании разнопородных мышей самец всегда выбирает для спаривания самку, отличающуюся от него по всем антигенам тканевой совместимости. Обонятельные реакции определяются особыми генами, которые, как выяснилось, находятся среди локусов тканевой совместимости. А это уже подход к иммунологическому анализу действия дистантных раздражителей и обонятельного предпочтения.
Феромоны у животных контролируют жизненно важные процессы, реакции поведения (сигналы агрессии, паники, "рабовладельческий" инстинкт, коллективные усилия) и защитные процессы. Феромоны называют гормонами среды, общения. У человека пока феромоны не найдены. Но кто знает, возможно, завтра не будет казаться нарочитой постановка вопроса об иммунологии человеческого поведения, общения, любви и даже таинств искусства?..
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'