Глава 8. Новообразования наружных половых органов (Михайличенко В.В.)
Опухоли полового члена
Доброкачественные опухоли. Доброкачественные новообразования полового члена делятся на эпителиальные и неэпителиальные. Неэпителиальные доброкачественные опухоли полового члена встречаются довольно редко и могут происходить из любой ткани. Это гемангиомы, лимфангиомы, нейрофибромы, фибромы, липомы, миомы, энхондромы кавернозных тел и др. Диагностика основывается на визуальном исследовании, пальпации и биопсии. Заболевание может вызывать косметический дефект, искривление полового члена, боли, реже - нарушение эрекции. С дифференциальнодиагностической целью показано гистологическое исследование биопсийного материала. Наличие доброкачественной опухоли позволяет проводить органосохраняющее хирургическое лечение (иссечение ее в пределах здоровых тканей). Большинство эпителиальных опухолей полового члена расцениваются как предраковые заболевания.
Папилломы - наиболее часто встречающиеся эпителиальные новообразования. Среди папиллом могут быть выделены вирусные и невирусные. Вирусные папилломы, или остроконечные кондиломы, представляют, в сущности, самостоятельную венерическую болезнь [Баженова А. А., Шабад А. Л., 1975]. Вирусная природа остроконечных кондилом была доказана прививкой бесклеточного фильтрата. Контагиозность и распространение этого заболевания половым путем подтверждены Б. А. Теохаровым (1962), А. Л. Шабадом (1963). Из-за длительности инкубационного периода, который составляет от 1 до 6 мес, не всегда представляется возможность установить источник заражения. Диагностика заболевания не представляет трудностей. Вирусные папилломы появляются у мужчин спустя 1-6 мес после случайной половой связи. Остроконечные кондиломы развиваются на головке полового члена и на внутреннем листке крайней плоти. Преимущественное место их локализации - венечная борозда, область уздечки, наружное отверстие уретры, ладьевидная ямка. Вначале кондиломы имеют диаметр около 0,1 мм. Затем они увеличиваются и приобретают характерный вид. Это ворсинчатые, остроконечные, безболезненные образования, как правило, множественные. Иногда, сливаясь, они достигают огромной величины. Поверхность кондилом сухая или влажная, легкоранимая. Располагаются они поверхностно, и основание их не имеет признаков инфильтрации. Однако при присоединении инфекции кондиломы могут некротизироваться, распадаться и изъязвляться. Возникает воспаление окружающих тканей, присоединяются зуд, боль, гноетечение из препуциального мешка, воспалительная реакция регионарных лимфатических узлов. В таком случае бывает трудно отличить кондилому от рака полового члена. Окончательный диагноз устанавливается при гистологическом исследовании биопсийного материала. В типичном случае обнаруживаются сравнительно тонкий слой эпителия без признаков гиперкератоза, хорошо развитая соединительнотканная строма с обильной сосудистой сетью и межклеточным отеком мальпигиева слоя.
Лечение. Мелкие вирусные папилломы полового члена (диаметром от 1 до 2 мм) можно подвергать электрокоагуляции. В остальных случаях показано их иссечение электроножом под местной инфильтрационной анестезией. При обширных разрастаниях вирусных папиллом на внутреннем листке крайней плоти следует произвести круговое иссечение ее. Во всех случаях обязательным является гистологический контроль.
Профилактика вирусных папиллом заключается в личной гигиене, в упорядочении половой жизни и выявлении источника заражения.
Предраковые заболевания. Невирусные папилломы являются предраковым заболеванием и развиваются в закрытом препуциальном мешке при фимозе. Они могут локализоваться на венечной борозде, вблизи ее на головке и на внутреннем листке крайней плоти. Они имеют широкое подвижное основание и ворсинчатую поверхность или грибовидную форму. Инфильтрация подлежащего участка кожи определяется при присоединении инфекции или при малигнизации. Папилломы невирусного происхождения диагностируются крайне редко, так как скрыты крайней плотью, развиваются бессимптомно и распознаются уже в стадии малигнизации. Окончательный диагноз может быть установлен только при биопсии. При гистологическом исследовании в редких наблюдениях обнаруживают строение типичной кожной папилломы. Чаще выявляются признаки малигнизации. В случае диагностирования типичной невирусной папилломы показано иссечение ее в пределах здоровых тканей. Профилактика невирусных папиллом заключается в гигиене препуциальной полости и раннем устранении фимоза.
Кожный рог. По внешнему виду напоминает рог животных или гипертрофированный ноготь. Выпуклая поверхность гладкая, плотная. Вогнутая сторона хрупкая, крошащаяся. Заболевание развивается при склонности организма к кератозам. Кожный рог представляет собой гиперплазию и метаплазию сосочкового слоя кожи. Эпителиальные тяжи клеток могут врастать в подлежащую ткань и малигнизироваться.
Эритроплазия Кейра. Заболевание начинается с появления на головке полового члена ярко-красной бляшки с бархатистой, слегка шероховатой поверхностью. Формы и размеры образования долго не изменяются. При гистологическом исследовании в типичных случаях выявляются гипоплазия зернистого и рогового слоев и васкуляризация подлежащей ткани. Эпителиальные клетки имеют веретенообразную или овальную форму. При малигнизации наблюдаются атипизм и полиморфизм клеток. Малигнизация эритроплазии начинается с изъязвления папилломатозных пролифераций.
Лейкоплакия. Это белесоватые участки с гладкой поверхностью и строго очерченными границами, которые появляются на головке полового члена, вокруг наружного отверстия мочеиспускательного канала и нередко распространяются на ладьевидную ямку. Лейкоплакия возникает вследствие очагового гиперкератоза. На поверхности, пораженной лейкоплакией, нередко появляются трещины, изъязвления, которые рубцуются и нередко приводят к сужению наружного отверстия уретры. Диагноз подтверждается гистологическим исследованием биопсийного материала. Выявляются хроническое воспаление, гиперкератоз, васкуляризация подлежащей ткани, лимфоцитарная инфильтрация.
Лечение предраковых заболеваний полового члена начинают после обязательной биопсии пораженного участка, с помощью которой окончательно устанавливается возможность малигнизации. При отсутствии злокачественного перерождения проводят органосохраняющее оперативное лечение (иссечение новообразования в пределах здоровых тканей, циркумцизию). При упорном рецидивировании заболевания производят резекцию или ампутацию головки полового члена в сочетании с близкофокусной рентгенотерапией. Лучевая терапия может применяться как самостоятельный метод лечения при лейкоплакии полового члена ввиду трудности оперативного удаления пораженного участка. Больные с предраковыми заболеваниями должны пройти соответствующее лечение и находятся на диспансерном учете. Профилактика заключается в ликвидации фимоза и соблюдения гигиены.
Злокачественные опухоли делятся на эпителиальные (раки) и неэпителиальные (сосудистые, соединительнотканные, пигментные опухоли и др.).
Злокачественные опухоли неэпителиального происхождения встречаются крайне редко. В мировой литературе имеется менее 100 наблюдений [Баженова А. П., Шабад А. Л., 1975]. Среди злокачественных опухолей неэпителиального происхождения чаще других возникают саркомы (ангиосаркомы, миосаркомы, нейросаркомы). Реже выявляются пигментные опухоли (меланосаркомы, меланомы), которые возникают из пигментных пятен и пигментированных папиллом кожи полового члена. Диагностика основывается на анамнезе, пальпации и цитологическом исследовании или биопсии. Биопсия абсолютно противопоказана при пигментных опухолях из-за опасности бурной диссеминации опухолевых клеток.
Клинически опухоль определяется как плотный узел в кавернозном теле головки полового члена. Нередко наблюдаются отечность, болезненность, нарушение половой функции. Частым симптомом опухоли кавернозных тел является приапизм. Опухоли метастазируют, как правило, в регионарные, но могут появляться и в отдаленных лимфатических узлах. Меланомы и меланосаркомы быстро прорастают кавернозные тела и сосуды, в связи с чем уже на ранних этапах развития появляются метастазы в легких, печени, костях и других органах.
Лечение должно быть комбинированным. Хирургическое лечение заключается в ампутации полового члена и двусторонней пахово-бедренной лимфаденэктомии. После операции проводят облучение области культи полового члена и паховых областей. Прогноз в большинстве случаев неутешителен. Лишь при своевременном оперативном вмешательстве он относительно благоприятен.
Рак. Среди злокачественных образований полового члена чаще других встречается рак. В нашей стране рак полового члена составляет 0,5% от всех раковых заболеваний у мужчин. В Европе и Северной Америке он встречается примерно в 1% от всех раковых заболеваний у мужчин, в то время как в странах Азии, Африки и Латинской Америки занимает одно из первых мест среди онкологических заболеваний у мужчин.
Этиология рака полового члена недостаточно ясна. Возникновение его большинство исследователей связывают с воздействием на кожу головки полового члена или внутреннего листка крайней плоти разлагающейся смегмы, обладающей канцерогенными свойствами. Смегма вырабатывается железами, расположенными в области венечной борозды и внутреннего листка крайней плоти. Канцерогенное действие смегмы неоднократно доказано в эксперименте.
Определенное значение придается описанным выше предраковым заболеваниям, особенно папилломам, лейкоплакии, кожному рогу, эритроплазии Кейра и др.
В патогенезе рака полового члена основное значение принадлежит застою содержимого препуциального мешка, возникающему чаще всего при фимозе. Присоединение инфекции, длительные воспаления, скопление продуктов распада смегмы способствует развитию заболевания. Поэтому у 60-80% больных раком полового члена наблюдается врожденный фимоз.
Патологическая анатомия. Типичным местом локализации рака полового члена являются венечная борозда, головка полового члена, внутренний листок крайней плоти. Опухоль имеет тенденцию распространяться контактным путем с головки на препуциальный мешок, прорастая его, и наоборот. Прорастание кавернозных тел наблюдается редко.
Различают 2 макроскопические формы рака полового члена - экзофитную (папиллярная, грибовидная) и эндофитную (узловатая, язвенная). А. П. Баженова и А. Л. Шабад (1975) считают, что любая форма рака при распаде может приобрести язвенный характер.
Особенностью рака полового члена являются воспалительные изменения в самой опухоли, а также гиперпластические процессы в окружающих тканях. Микроскопически рак полового члена представляет собой плоскоклеточный рак с той или иной степенью ороговения.
Клиническая картина. Начальные стадии рака полового члена протекают скрыто, как правило, внутри крайней плоти при фимозе. Заболевание может начинаться с появления папилломы, эрозии, язвочки, уплотнения, которые не причиняют физических страданий больному. Присоединение инфекции, распад опухоли, прорастание ее в крайнюю плоть, появление жжения, зуда, значительное увеличение головки полового члена приводят больного к врачу. Рост опухоли или распространение воспалительного инфильтрата могут вызвать сдавление наружного отверстия уретры и странгурию. Поражение кавернозных тел проявляется болезненной эрекцией, а иногда приапизмом. Регионарными лимфатическими узлами, куда прежде всего метастазирует рак полового члена, являются пахово-бедренные и подвздошные. Однако примерно в 50% наблюдений увеличение регионарных лимфатических узлов обусловлено воспалительной инфильтрацией в раковой опухоли и окружающих тканях. Метастазы в отдаленные органы (печень, легкие) при раке полового члена редки.
При прорастании кавернозных тел метастазы могут распространяться в глубокие тазовые и подвздошные лимфоузлы.
Классификация. Злокачественные опухоли полового члена классифицируются по системе TNM.
Т - первичная опухоль: Т1 - опухоль менее 2 см в диаметре, без инфильтрации; Т2 - опухоль размерами от 2 до 5 см с незначительной инфильтрацией подлежащих тканей; Т3 - опухоль размерами более 5 см или меньше, но с прорастанием пещеристых тел; Т4 - опухоль прорастает в соседние ткани и органы. N - метастазы в лимфатические узлы (оцениваются по локализации и смещаемости: N1 - увеличенные, смещаемые паховые лимфоузлы с одной стороны; N2 - увеличенные, смещаемые паховые лимфоузлы с обеих сторон; N3 - увеличенные с обеих сторон несмещаемые паховые лимфоузлы; М - метастазы в отдаленные органы: М0 - метастазы в отдаленные органы отсутствуют; Ml - метастазы в отдаленные органы имеются.
Диагностика рака полового члена нередко затруднена. Окончательный диагноз ставится на основании данных биопсии органа, а также увеличенных лимфоузлов или цитологического изучения их пунктата. Следует проводить дифференциальную диагностику рака с рядом воспалительных заболеваний (туберкулез, сифилис, язвенный баланопостит), с предраком полового члена. В таких случаях помогают цитологическое исследование мазков-отпечатков, проведение специфических реакций (Манту, Вассермана) и биопсии, при которой кусочки ткани следует брать из глубины опухоли.
Лечение рака полового члена зависит от стадии, проводится с учетом прорастания и инфильтрации тканей полового члена, а также от наличия метастазов. Применяются лучевая или радиевая терапия, хирургическое лечение (удаление опухоли и лимфогенных метастазов) и комбинированный метод с использованием лучевого воздействия и оперативного вмешательства. В начальных стадиях рекомендуются циркумцизия и проведение близкофокусной или радиевой (внутритканевой, аппликационной) терапии. Круговое иссечение крайней плоти также оправдано при расположении опухоли в ее листках. При ограниченном росте опухоли показано иссечение ее электроножом в пределах здоровых тканей. При интактной головке полового члена рекомендуется операция Сапожкова (полное удаление кожи полового члена с погружением скальпированного полового члена под кожу мошонки). Применяется также резекция головки или части полового члена по В. Н. Шевкуненко. Однако все большее признание получает комбинированное лечение рака полового члена.
При прорастании опухоли в кавернозные тела при наличии метастазов в регионарные лимфоузлы показаны близкофокусная рентгенотерапия или телегамматерапия на первичную опухоль с последующей ампутацией полового члена и двусторонней пахово-бедренной лимфаденэктомией (операцией Дюкена). В более запущенных случаях удаляются не только пахово-бедренные, но и подвздошные лимфоузлы. А. И. Страшинин (1953) рекомендует облучать одновременно первичную опухоль и пахово-бедренную область, укладывая половой член на соответствующую паховую область.
Прорастание рака полового члена в органы мошонки является показанием к эмаскуляции - удалению единым блоком полового члена, мошонки, яичек с придатками и подшиванию уретры в линию шва. При наличии единичных отдаленных метастазов возможно их оперативное удаление. При множественных отдаленных метастазах показаны паллиативные операции, химиотерапия, которая в отдельных случаях может продлить больным жизнь. Оперативное лечение сочетается с пред- и послеоперационной лучевой терапией на область первичного опухолевого очага и регионарных лимфатических узлов.
Прогноз зависит от стадии заболевания. При комплексном лечении 5-летняя выживаемость наблюдается у 60-70% больных. При наличии регионарных метастазов прогноз чаще неблагоприятный.
Профилактика рака полового члена заключается в тщательном соблюдении гигиены препуциального мешка, в ранней ликвидации фимоза, в своевременном выявлении и лечении предраковых заболеваний.
Опухоли мочеиспускательного канала
Опухоли мочеиспускательного канала делятся на доброкачественные и злокачественные. Наиболее часто они встречаются в возрасте 20-30 лет.
Доброкачественные опухоли могут исходить из слизистой оболочки уретры и ее желез (папилломы, полипы, остроконечные кондиломы) или же берут свое начало из других тканей (фибромы, миомы, фибромиомы, нейрофибромы, ангиомы).
Папилломы уретры - это сосочковые образования с ворсинчатой поверхностью, располагающиеся на широком основании или длинной ножке одиночно или группой по задней стенке уретры у наружного ее отверстия. Папилломы, как правило, имеют мягкоэластическую консистенцию и четко отграничены от окружающей слизистой оболочки.
Ангиомы образуются в результате гиперплазии капилляров, представляют собой синевато-красные образования, бледнеющие при надавливании, располагающиеся у наружного отверстия уретры. Ангиомы следует различать с варикозно-расширенными венами подслизистого слоя, которые могут обнаруживаться по всему просвету уретры, но чаще всего в предстательной ее части у семенного бугорка. Варикозно-расширенные вены мочеиспускательного канала могут быть причиной гематоспермии.
Фибромы, миомы, фибромиомы встречаются у мужчин очень редко. Развиваясь в фиброзно-мышечном слое уретры, они выпячиваются на ножке в просвет ее. Консистенция их плотная, эластическая; несмотря на то, что они растут медленно, могут вызывать расстройства мочеиспускания.
Клиническая картина доброкачественных опухолей уретры зависит от их локализации. Основными симптомами заболевания являются расстройства мочеиспускания (затрудненное мочеиспускание, разбрызгивание струи, учащенные позывы); гематурия (начальная и терминальная). С присоединением инфекции возможно появление дизурии и гнойных выделений из уретры. При поражении задней части уретры наблюдается еще более выраженная дизурия, могут появляться болезненные семяизвержение, гематоспермия, беспричинные эрекции, приапизм.
Диагностика основана на тщательном осмотре и пальпации полового члена, уретроскопии. При невозможности проведения уретроскопии показана уретрография. В некоторых случаях для дифференциальной диагностики требуется биопсия.
Лечение доброкачественных опухолей должно быть радикальным. Следует иссекать опухоль в пределах здоровых тканей. При расположении опухоли у наружного отверстия мочеиспускательного канала возможно ее иссечение под местной новокаиновой анестезией. При наличии опухоли в проксимальных отделах уретры показана резекция уретры вместе с опухолью. Значительные трудности представляет хирургическое лечение распространенного папилломатоза уретры. В то же время паллиативные мероприятия (прижигания растворами серебра нитрата и поверхностная электрокоагуляция) приводят лишь к временному эффекту и грозят малигнизацией опухоли. Поэтому нередко приходится прибегать к резекции висячей части уретры. При радикальном лечении прогноз благоприятный.
Злокачественные опухоли. Рак мочеиспускательного канала относится к редким заболеваниям. Этиология его пока остается неясной. Факторами, способствующими его возникновению, считают уретриты, стриктуры, свищи. Иногда малигнизации подвергаются некоторые доброкачественные новообразования уретры, гиперкератозы. У большинства больных рак развивается из слизистой оболочки кавернозной части уретры на фоне лейкоплакии и плоскоклеточной метаплазии и поэтому почти всегда является плоскоклеточным, с ороговением и без него.
Выделяют 2 макроскопические формы рака мужской уретры: ворсинчатую и инфильтрирующую. Опухоль может поражать пенальную бульбо-мембранозную и предстательную части уретры. Чаще рак поражает бульбо-мембранозную часть и переднюю часть уретры, гораздо реже располагается в предстательной ее части. В начале развития опухоли мочеиспускательного канала могут метастазировать в паховые лимфатические узлы. Прорастание опухолью спонгиозного тела и окружающих тканей, особенно в бульбо-мембранозной части уретры, может сопровождаться появлением метастазов в тазовых и забрюшинных лимфатических узлах.
Клиническая картина может зависеть от основного заболевания уретры, на фоне которого возникает рак (стриктура, хронический уретрит, наличие доброкачественной опухоли уретры). При первичном заболевании симптоматика вначале скудная. Отмечаются жжение, зуд в уретре, нестойкая дизурия. Затем эти явления становятся постоянными, затрудняется мочеиспускание. Появляются выделения из уретры (вначале серозные, затем кровянистые или гнойные при инфицировании слизистой оболочки). Могут иметь место мучительные эрекции. Рост опухоли сопровождается инфильтрацией окружающих тканей, возникновением конгломератов плотных узлов в паховых областях, которые могут быть поражены не только бластоматозным, но и воспалительным процессом. Появляются постоянные боли в промежности. Может наступить задержка мочи, при которой катеризация сопровождается уретроррагией. Непроходимость уретры ведет к мочевой инфильтрации, образованию абсцессов и свищей. Моча становится мутной и зловонной. Постепенно опухоль разрушает наружные половые органы, может переходить на предстательную железу, промежность, лобковые и седалищные кости. В этом периоде метастазы появляются в тазовых, забрюшинных лимфоузлах, а также в легких, печени и других органах. Блокирование лимфатических путей приводит к отеку мошонки и полового члена.
Диагностика рака мочеиспускательного канала в начальном периоде его развития затруднена. Важное значение имеют осмотр, пальпация, цитологическое исследование отделяемого из уретры, уретроскопия, уретрография, биопсия. Экскреторная урография, лимфография и флебография, УЗИ и ядерно-магнитнорезонансная томография позволяют диагностировать метастазы.
Лечение рака мочеиспускательного канала комбинированное. Применяются хирургические методы и лучевая терапия. При поражении ладьевидной ямки производится частичная ампутация полового члена с захватом 1,5-2 см здоровых тканей. При расположении опухоли в пенальной части уретры рекомендуется ампутация полового члена. При поражении бульбо-мембранозной части мочеиспускательного канала показана эмаскуляция (удаление полового члена, мошонки и ее органов) с промежностной уретрокутанеостомией. Оперативное лечение следует сочетать с лучевой терапией на послеоперационный рубец (от 20 до 30 Дж/кг). Если после удаления первичного очага опухоли паховые лимфатические узлы уменьшаются, становятся мягкими и подвижными, то это свидетельствует о воспитательной аденопатии. Плотные малоподвижные безболезненные лимфатические узлы подлежат оперативному удалению (операция Дюкена) с последующей лучевой терапией.
Прогноз при раке мочеиспускательного канала неблагоприятный ввиду появления у большинства больных метастазов в первую половину года после операции.
Профилактика рака уретры состоит в своевременном лечении воспалительных заболеваний, стриктур мочеиспускательного канала и радикальном удалении доброкачественных опухолей ее.
Опухоли мошонки
Первичные опухоли мошонки являются редким заболеванием. В отечественной литературе описаны единичные наблюдения доброкачественных опухолей мошонки: лимфангиомы [Гораш В. А., 1909], гемангиомы [Гурецкий Л. А., 1936], хондрофибромы [Гольдин Г. И., 1937], фибромиомы [Жиляев И. Ф., 1938], липомы [Донин В. И., 1958]. Гораздо чаще на мошонке наблюдаются серозные, атероматозные и дермоидные кисты [Айдаров А. А., 1977].
Злокачественные опухоли мошонки также встречаются не часто. А. П. Баженова, А. Л. Шабад (1975) за 10 лет приводят лишь 3 наблюдения злокачественных опухолей мошонки. Чаще других встречаются опухоли эпителиального происхождения, в основном плоскоклеточный рак, который описан у мужчин с мацерациями мошонки при наличии мочевых и гнойных свищей. Рак мошонки довольно быстро метастазирует в пахово-бедренные лимфатические узлы. Значительно реже имеют место саркоматозные опухоли мошонки (липосаркома, рабдомиосаркома, лейомиосаркома).
Следует помнить о том, что иногда возможны переход раковой опухоли полового члена на кожу мошонки, прорастание мошонки злокачественным новообразованием, исходящим из яичка или его придатка, а также метастазирование опухолей внутренних половых органов.
Лечение. Доброкачественные опухоли подлежат оперативному вылущиванию или иссечению с последующим обязательным гистологическим исследованием. При злокачественных новообразованиях применяется комбинированное оперативное лечение. При поражении опухолью только кожи ограничиваются иссечением первичного очага с захватом здоровой кожи в пределах 5 см. При прорастании новообразования в клетчатку и оболочки яичка необходимо удаление половины мошонки с ее содержимым (гемискроторхиэктомия). Если опухоль переходит на противоположную сторону мошонки, то возможно ее полное удаление с последующей пластикой кожного дефекта. Пахово-бедренную лимфаденэктомию (операцию Дюкена) производят на стороне поражения или с обеих сторон. Оперативное удаление опухоли во всех случаях сочетают с лучевой терапией на область первичного очага и метастазов.
Профилактика заключается в личной гигиене, в своевременном выявлении и оперативном лечении доброкачественных опухолей мошонки.
Опухоли яичка
Доброкачественные опухоли яичка являются казуистической редкостью и составляют лишь 0,8% от всех новообразований. Среди них встречаются тератома, липома, хондрома и фибромиома. Однако все эти опухоли следует считать потенциально злокачественными, так как они могут малигнизироваться.
Поданным Е. Б. Маринбаха (1972 г), в 98,2% случаев опухоли яичка являются злокачественными. Они составляют 1-2% от всех злокачественных новообразований у мужчин, занимая по частоте одно из последних мест в онкологии. Чаще опухоль возникает в возрасте от 17 до 45 лет, т. е. в период наибольшей гормональной и репродуктивной активности, и значительно реже наблюдается у детей и стариков.
Этиология. Экспериментальными работами И. О. Михаловского (1928), В. М. Бреслера (1959), В. П. Коноплева (1963), клиническими наблюдениями И. Ф. Юнды (1967), Л. П. Имшинецкой (1970), В. И. Шилова (1961), Е. Б. Маринбаха (1972) показано, что ведущим фактором в возникновении злокачественных опухолей яичка являются гормональные нарушения во взаимодействии между гонадотропной функцией гипофиза и функцией яичка.
Гипогонадизм вызывает растормаживание гипоталамо-гипофизарной системы, что ведет к повышенной выработке гонадотропинов, которые усиливают стимуляцию яичек. Гиперстимуляция гонадотропинами способствует атипическому росту и развитию в яичке злокачественной опухоли. Гипогонадные состояния могут быть врожденными (крипторхизм, рудиментарные яички, гипоплазия, дисгенезия половых желез и др.) или приобретенными (вследствие перенесенных орхитов, различных видов травм, интоксикаций и др.).
По нашим данным, в качестве предшествующих заболеваний у больных со злокачественными опухолями яичек наиболее часто выявлялись крипторхизм, травма (в том числе предшествующие операции в пахово-мошоночной области) и воспалительные заболевания яичек с последующей гипоплазией.
Патологическая анатомия. По морфологическим признакам злокачественные новообразования яичка делят на 2 группы: герминогенные и негерминогенные.
Герминогенные опухоли развиваются из клеток семенного эпителия. Негерминогенные опухоли происходят из других элементов ткани яичка. Частота герминогенных опухолей составляет 95-97%. Эти новообразования часто имеют неоднородную структуру, встречаются комбинации нескольких видов опухолей. Поэтому для удобства клиницистов, руководствуясь клинико-морфологическим принципом с учетом чувствительности к лучевой терапии и различным химиопрепаратам, Е. Б. Маринбах объединяет многочисленные варианты герминогенных опухолей яичек в 4 группы: 1) семинома, 2) тератобластома и (или) эмбриональный рак с семиномой или без нее, 3) тератобластома и(или) эмбриональный рак и хорионэпителиома с семиномой или без нее, 4) хорионэпителиома с семиномой или без нее.
Семинома - плотная дольчатая опухоль, чаще беловато-серого цвета с блестящей на разрезе поверхностью, происходящая из эпителия семенных канальцев. При гистологическом исследовании в ткани типичной семиномы обнаруживаются крупные с округлыми очертаниями клетки, в которых видны большие центрально расположенные ядра. В строме опухоли отмечаются лимфоидная инфильтрация и гранулематозная реакция. Вариантами семиномы являются анапластическая семинома, отличающаяся клеточным полиморфизмом, и сперматоцитарная семинома, состоящая из клеток, напоминающих сперматогонии и сперматоциты.
Хорионэпителиома относится к наиболее злокачественным опухолям яичка, отличается быстрым ростом с разрушением сосудов и образованием очагов геморрагического некроза. Опухоль плотная, поверхность разреза представляется пестрой. По микроскопическому строению имеет сходство с ворсинками хориона или может характеризоваться цито- или синцитиотрофобластической дифференцировкой.
Тератобластома - плотная, бугристая опухоль. На поверхности разреза определяются множественные кисты, наполненные желтоватой жидкостью или кровью. Тератобластома может развиваться из всех 3 зародышевых листков. При микроскопическом исследовании определяются элементы тератомы (дифференцированная ткань эктодермы, эндодермы или мезодермы), одновременно обнаруживаются и участки недифференцированной ткани.
Анапластическая тератобластома (эмбриональный рак) имеет мягкую консистенцию и пеструю поверхность среза из-за наличия участков некроза. Относится к наиболее зрелым опухолям и состоит из низкодифференцированных, атипичных клеток, которые образуют эпителиальные пласты или железистые структуры.
Негерминогенные опухоли могут быть специфическими и неспецифическими и составляют 3-4% всех новообразований яичка.
Специфические негерминогенные опухоли исходят из специфических элементов ткани яичка. Выделяют лейдигому, возникающую из гландулоцитов яичка, и сертолиому, которая образуется из сустентоцитов.
Неспецифические негерминогенные опухоли берут начало из сосудов, нервов и других элементов стромы (рабдомиосаркома, миксофибросаркома, ретикулосаркома и др.). Крайне редко наблюдаются опухоли вторичные, в яички может метастазировать рак предстательной железы.
Большинство опухолей метастазируют лимфогенным путем. Гематогенное метастазирование характерно для хорионэпителиомы, способной к инвазии в кровеносные сосуды. Злокачественные опухоли яичка имеют тенденцию к быстрому метастазированию. По данным D. Skinner и соавт. (1981), в момент обращения у 25% больных с семиномой и 66% больных с несеминомными опухолями определяются регионарные и отдаленные метастазы. В первую очередь метастазами поражаются регионарные лимфатические узлы, расположенные в зоне эмбриональной закладки яичек, в области почечных сосудов, спереди от аорты и нижней полой вены до уровня отхождения нижней брыжеечной артерии. Во вторую очередь метастазы появляются в лимфатических узлах, расположенных вдоль дистальной части брюшной аорты и по ходу подвздошных сосудов. Далее опухоль может метастазировать в средостение, легкие, мозг, кости, печень и другие органы, так как по лимфатическим путям опухолевидные эмболы попадают в грудной проток, венозную систему и общий кровоток (вторичное гематогенное распространение метастазов). Наиболее злокачественные элементы опухоли метастазируют раньше других. Поэтому нельзя по гистологической структуре метастазов судить о строении первичной опухоли.
Клиническая картина. Опухоль яичка чаще развивается незаметно для больного. Клиническая картина характеризуется наличием местных, общих и редких симптомов заболевания. Первым проявлением заболевания может быть чувство дискомфорта, тяжести, давления в пораженном яичке. Позднее появляется боль, которая является следствием значительного повышения внутритестикулярного давления, прорастания белочной оболочки яичка или элементов семенного канатика и нередко служит признаком запущенности заболевания. Боль может иррадиировать в пах, бедро и поясницу еще до появления метастазов. Указанные местные симптомы приковывают внимание больных, и они могут обнаружить у себя уплотнение или опухоль яичка. По мере роста опухоли яичко увеличивается, становится плотным, бугристым; появляется спаянность с кожей мошонки. При крипторхизме заболевание проявляется болью, припухлостью и уплотнением в проекции яичка. Опухоль нередко сопровождается вторичной водянкой оболочек яичка, что значительно затрудняет диагностику. Постепенно присоединяются общие симптомы заболевания: слабость, вялость, повышенная утомляемость, субфебрильная температура тела. Могут иметь место и гормональные нарушения, которые проявляются понижением половой активности, гинекомастией. При лейдигоме, продуцирующей андрогены, наблюдается преждевременное половое созревание. Сертолиома может сопровождаться гиперэстрогенемией, признаками феминизации.
Метастазирование опухоли в регионарные и отдаленные лимфоузлы и органы проявляется отеками нижних конечностей, варикоцеле, гематурией, желтухой и другими редкими симптомами.
Классификация. Опухоли яичка классифицируются по системе TNM.
Т - первичная опухоль: Т1 - опухоль не выходит за пределы белочной оболочки и не деформирует яичко; Т2 - опухоль деформирует яичко, не прорастая белочную оболочку; Т3 - опухоль выходит за пределы белочной оболочки, прорастая придаток; Т4 - опухоль прорастает мошонку. N - метастазы в регионарные лимфоузлы: N1 - регионарные метастазы не прощупываются, но обнаруживаются рентгенологически; N2 - регионарные метастазы прощупываются. М - отдаленные метастазы: Ml -метастазы в отдаленных лимфоузлах; М2 - метастазы в отдаленных органах; М3 - метастазы в отдаленных лимфатических узлах и органах.
Диагностика складывается из данных анамнеза, осмотра, пальпации, лабораторных исследований, радионуклидной диагностики, УЗИ, ядерно-магнитнорезонансной томографии для диагностики метастазов и биопсии.
В большинстве наблюдений осмотр и пальпация позволяют установить наличие опухоли яичка. При этом у 10-15% больных выявляются увеличение и болезненность молочных желез (гинекомастия). При поражении неопустившегося яичка решение вопроса о наличии опухоли затрудняется. При этом необходимо тщательно осмотреть и пальпировать область пахового канала, а также подвздошную область в положении стоя, в расслабленном состоянии и при напряжении брюшного пресса. Наличие водянки оболочек яичка также затрудняет диагностику. При этом следует произвести диафаноскопию мошонки. При подозрении на опухоль рекомендуется пункция оболочек яичка с последующей пальпацией его и обязательным цитологическим исследованием полученной жидкости. Пальпацию забрюшинных лимфатических узлов и области ворот почки (пути лимфогенного метастазирования) производят обычно натощак, после опорожнения кишечника с помощью клизмы, поставленной накануне вечером и утром в день обследования.
Клинические исследования крови и мочи не отражают особенности опухолевого процесса. Из лабораторных методов исследования при диагностике опухолей яичка имеет значение определение хорионического гонадотропина в моче и эмбриоспецифического γ-глобулина (фетопротеина) в крови больных. Высокая экскреция с мочой хорионического гонадотропина (свыше 100 МЕ/л) характерна для хорионэпителиомы яичка или неоднородной опухоли, содержащей элементы хорионэпителиомы. Е. Б. Маринбах (1975) обнаруживал отсутствующий в норме фетопротеин в крови у больных с опухолями яичка неоднородного строения, в то время как у больных семиномой и негерминогенными опухолями фетопротеин не определяется.
Рентгенорадионуклидная диагностика служит для выявления регионарных и отдаленных метастазов. Применяются обзорная и экскреторная урография, венокаваграфия, аортография, лимфаденоангиография, рентгеноскопия и обзорная рентгенография грудной клетки, а также радионуклидная лимфография и лимфосканирование.
На экскреторных урограммах при наличии забрюшинных метастазов могут определяться отклонение мочеточника в латеральную сторону и сдавление его с развитием уретерогидронефроза. Венокаваграфия позволяет обнаружить даже сравнительно небольшие метастазы в паракавальные лимфатические узлы при поражении правого яичка. Выявляются дефекты наполнения, смещения нижней полой вены и др. Аортография показана для определения парааортальных метастазов при опухолях левого яичка. Однако упругая, плотная стенка аорты с трудом деформируется и поэтому при помощи аортографии можно выявить лишь большие опухолевые инфильтраты.
Лимфанигиоаденография позволяет при опухолях яичка получить наиболее точную информацию о состоянии забрюшинных путей лимфооттока. Наличие метастазов в регионарных лимфатических узлах определяется по дефекту наполнения контрастированного лимфатического узла и блокаде лимфатических сосудов с появлением извращенного лимфооттока, коллатералей. Более точное представление о состоянии забрюшинных узлов можно получить при двусторонней лимфангиоаденографии.
Радионуклидная лимфография и лимфосканирование применяется для диагностики метастазов семиномы и опухолей неоднородного строения с элементами семиномы.
Для диагностики метастазов опухоли яичка в отдаленные лимфоузлы и органы широко применяются рентгеноскопия и рентгенография органов грудной клетки и брюшной полости, дополняемые томографией. Метастазы имеют вид одиночных или множественных круглых теней с четкими контурами. УЗИ, ядерно-магнитный резонанс тепловизионные исследования (телетермографии) могут быть использованы для распознавания опухолей крипторхического яичка (особенно при абдоминальной форме), а также метастазов различной локализации.
Цитологическое исследование пунктатов опухоли имеет своих сторонников и противников. При пункции опухоли появляется опасность ее диссеминации. Кроме того, пункционная биопсия не дает полного представления о морфологических особенностях опухоли, а отрицательный результат цитологического исследования не исключает наличия новообразования. Обязательному цитологическому исследованию следует подвергать водяночную жидкость из оболочек яичка, плевральную и асцитическую жидкость.
Окончательный диагноз и гистологическая структура опухоли могут быть установлены лишь после биопсии. До получения результатов биопсии следует наложить зажим на семенной канатик для предотвращения распространения опухолевых эмболов.
Дифференциальную диагностику опухолей яичка приходится проводить со специфическими воспалительными заболеваниями яичка. При подозрении на бруцеллезный орхит диагноз уточняется с помощью реакции агглютинации по Райту - Хаддлсону, реакцией связывания комплемента и аллергической внутрикожной пробой. Туберкулезный орхит подтверждается туберкулезным поражением почек, предстательной железы, семенных пузырьков и положительными пробами Пирке, Манту.
При подозрении на люэтический процесс в яичке важную роль играют половой анамнез, реакция Вассермана. В сомнительных случаях для дифференциальной диагностики хронического орхита и опухоли яичка показано проведение экстренной открытой биопсии на операционном столе.
Лечение. Наиболее эффективным при всех видах злокачественных опухолей яичка показано комплексное лечение, которое включает хирургический, лучевой методы и химиотерапию.
Оперативное лечение злокачественных опухолей яичка преследует 2 цели: удаление первичной опухоли (орхифуникулэктомия) и удаление всей забрюшинной клетчатки с лимфатическими узлами на стороне поражения (внебрюшинная лимфаденэктомия). Орхифуникулэктомия может производиться под местной анестезией или наркозом. Производят послойный пахово-мошоночный разрез с обязательным вскрытием апоневроза над паховым каналом. Семенной канатик выделяют до внутреннего отверстия пахового канала, перевязывают и отсекают, после чего удаляют яичко со всеми оболочками. Пластику пахового канала производят по способу Мартынова или Кимбаровского.
Внебрюшинная лимфаденэктомия может быть выполнена из различных доступов. Шевассю после орхифуникулэктомии продолжал кожный разрез от глубокого пахового кольца вверх по направлению к концу X ребра. При необходимости разрез расширялся в медиальную сторону в поперечном направлении. Hinman для внебрюшинной лимфаденэктомии применял разрез, идущий от области поверхностного пахового кольца; параллельно и медиальнее передневерхней ости крыла подвздошной кости, дугообразно к концу XII ребра и далее на поясничную область параллельно XII ребру. Применяются также трансплевральный торакоабдоминальный разрез, доступ по Нагамацу и др. (рис. 47).
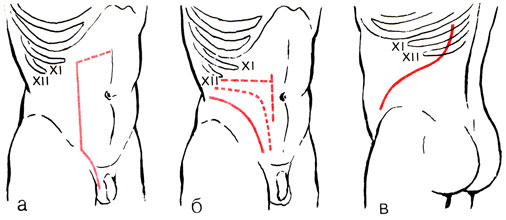
Рис. 47. Кожные разрезы при забрюшинной лимфаденэктомии. а - разрез по Шевассю; б - разрез по Хинману; в - трансплевральный торакоабдоминальный доступ (разрез по Куперу и соавт.)
После рассечения кожи, подкожной клетчатки и мышц передней брюшной стенки брюшину отодвигают медиально. На поверхности брюшины выделяют яичковую вену, которую удаляют вместе с клетчаткой, окружающей нижний полюс почки, и далее слева по ходу брюшной аорты - все лимфоузлы и жировую клетчатку, справа по ходу нижней полой вены до разветвления подвздошных сосудов (рис. 48). Операцию заканчивают оставлением в ране 2 резиновых дренажей.
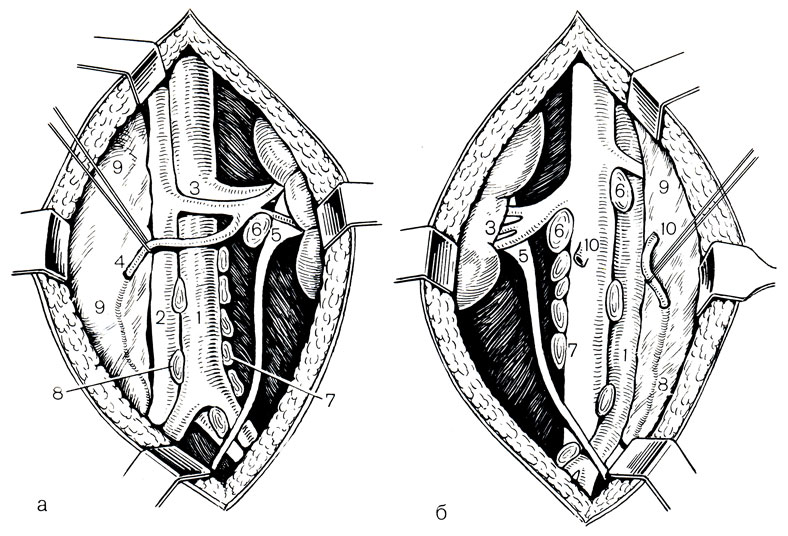
Рис. 48. Операция Шевассю. а - слева; б - справа. 1 - аорта; 2 - нижняя полая вена; 3 - почечная вена; 4 - яичковая вена; 5 - мочеточник; 6,7,8 - лимфатические узлы; 9 - париетальная брюшина; 10 - яичковая вена отсечена от нижней половой вены
Орхифуникулэктомия и внебрюшинная лимфаденэктомия в зависимости от состояния больного могут производиться одномоментно или в 2 этапа. Большинство клиницистов считают, что внебрюшинную лимфаденэктомию не обязательно проводить при семиноме, так как эта опухоль и ее метастазы весьма чувствительны к лучевому воздействию и химиотерапии. В последние годы появились сообщения об оперативном удалении одиночных метастазов в отдаленные органы (легкие, печень и др.).
Лучевая терапия показана при семиноме, ретикулосаркоме и опухолях неоднородного строения с элементами семиномы. В послеоперационном периоде лучевую терапию назначают сразу же после заживления раны. Облучают область послеоперационного рубца и метастазов. Применяется также послеоперационная лучевая терапия первичной опухоли при ее больших размерах или в тех случаях, когда опухолью поражается неопустившееся яичко (при паховой и брюшной ретенции). Разовая доза достигает 2-3 Дж/кг, суммарная - 40-60 Дж/кг.
Химиотерапия. В настоящее время имеется большое количество лекарственных веществ, применяемых для лечения злокачественных опухолей яичка. В Институте клинической и экспериментальной онкологии АМН СССР [Маринбах Е. Б., 1975] разработана схема сочетанной химиотерапии злокачественных опухолей яичка (таб. 1).
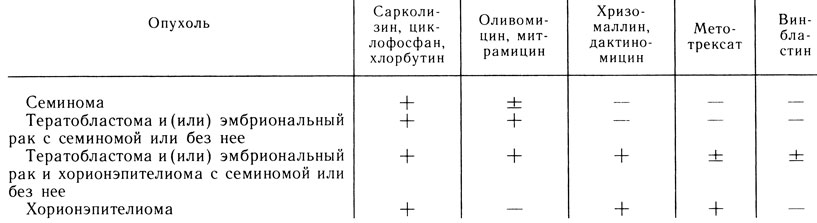
Таблица 1. Схема сочетанной химиотерапии герминогенных опухолей
Противоопухолевые средства как компоненты в сочетанной терапии метастазов опухолей яичка применяются в следующих дозировках. Сарколизин вводится внутривенно по 30-50 мг 1 раз в неделю (на курс 200-300 мг), циклофосфан - по 400 мг через день или по 1 г в 5-6 дней (на курс 8-12 г), хлорбутин - внутрь по 10 мг ежедневно (на курс 200-400 мг), оливомицин - внутривенно по 10-15 мг через день (на курс 150-200 мг), митрамицин - внутривенно по 25-30 мкг на 1 кг массы тела ежедневно (на курс 250-300 мкг), хризомалин и дактиномицин - внутривенно по 50 мкг через день (на курс 5-12 кг), метотрексат - внутрь по 5 мг ежедневно (на курс 100-150 мг), винобластин - внутривенно по 0,1-0,25 мг на 1 кг массы тела больного (на курс 1-2,5 мг). Схема может быть изменена в процессе лечения. При герминогенных опухолях яичка эффективны следующие препараты: алкилизирующие соединения (сарколизин, циклофосфан и фосфамид), антиметаболиты (метотрексат), противоопухолевые антибиотики (актиномицин Д, адриамицин, блеомицин, митрамицин), алкалоиды (винбластин, винкристин), а также препараты цистидиаминодихлорплатины (цисплатин, платидиам) и этопозид.
Возможность введения ударных доз химиопрепаратов появилась после освоения инфузионной эндолимфатической терапии. Отмечено быстрое рассасывание семиномных опухолевых конгломератов после эндолимфатического введения 200-250 мг сарколизина, растворенного в 20-22 мл изотонического раствора (2/3 дозы инфузировать на стороне поражения, 1/3 - на противоположной стороне). Осложнениями такой терапии являются лимфангит и отек нижних конечностей.
Метастазы негерминогенных новообразований яичка, как правило, устойчивы к существующим противоопухолевым препаратам.
Прогноз при злокачественной опухоли яичка зависит от морфологической структуры и распространенности процесса к моменту начала лечения. При семиноме прогноз более благоприятный, при других видах опухоли и особенно при хорионэпителиоме он значительно хуже.
Профилактика опухолей яичка заключается в раннем выявлении и правильном лечении крипторхизма и других аномалий яичка. Диспансерное наблюдение должно проводиться за больными с гипоплазией яичек, перенесшими орхипексию, и больными, получающими гормонотерапию. Важное значение в профилактике опухолей яичка имеет также предотвращение различного рода травм половых органов.
Опухоли придатка, оболочек яичка и семенного канатика
Новообразования придатка, оболочек яичка и семенного канатика встречаются довольно редко и по своему гистологическому строению чаще всего схожи между собой. Известны следующие доброкачественные и злокачественные опухоли: саркомы, фибромы, липомы, фиброаденомы, нейрофиброаденомы, миомы, миксомы, лимфангиомы, мезотелиомы, рак, дермоид и пр. Доброкачественные опухоли развиваются медленно и не достигают больших размеров. Злокачественное новообразование может прорастать яичко, метастазировать в паховые и забрюшинные лимфатические узлы.
Диагностика затруднена из-за бессимптомного течения. Основными признаками опухоли являются чувство дискомфорта, наличие уплотнения, укорочение семенного канатика (подтянутость яичка к паховому кольцу) на стороне поражения. Поверхность доброкачественных опухолей гладкая, злокачественных - бугристая. Чаще встречаются доброкачественные опухоли придатка, оболочек яичка и семенного канатика, а также поражение придатка яичка воспалительным процессом (кисты, эпидидимит). Поэтому нередко злокачественные новообразования указанных локализаций диагностируются лишь во время операции или гистологического исследования опухоли.
Лечение - хирургическое. Доброкачественные опухоли удаляют в пределах здоровых тканей. При злокачественных новообразованиях показана гемикастрация с максимально высоким удалением или облучением паховых и забрюшинных лимфатических узлов.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'