Глава 3. Эмбриология и пороки развития мужских половых органов (Михайличенко В.В.)
Эмбриогенез
Внутренние и наружные половые органы формируются у мужчин в эмбриональном периоде, в пубертатном - продолжается их развитие и совершенствование, заканчивающееся к 18-20 годам. В дальнейшем в течение 25-30 лет поддерживается нормальное функционирование половых желез, сменяющееся постепенным угасанием их функции и обратным развитием. Пол человека определяется прежде всего набором половых хромосом (хромосомный пол), от которых зависят формирование и построение половых желез, влияющих на гормональный пол, который, в свою очередь, определяет строение половых органов.
От последнего факта зависят воспитание индивида, психический и гражданский пол.
Внутриутробное половое развитие происходит в соответствии с генетическим (хромосомным) полом эмбриона. Хромосомный набор обусловливает направленную половую эволюцию и взрослого индивида. Половая клетка человека (мужская или женская) содержит 23 хромосомы (гаплоидный набор). Генетический, или хромосомный, пол определяется в момент оплодотворения и зависит от того, какой хромосомный материал получает яйцеклетка, которая в норме имеет 22 аутосомы и половую X-хромосому, при слиянии ее со спермием, содержащим 22 аутосомы и половую X- или Y-хромосому. При слиянии яйцеклетки со спермием, несущим половую X-хромосому, первичная половая железа эмбриона будет закладываться по женскому типу (яичники). При оплодотворении яйцеклетки спермием, содержащим половую Y-хромосому, первичная половая железа эмбриона будет развиваться по мужскому типу (яички). Нормальный мужской генотип, следовательно, определяется набором, состоящим из 44 аутосомных и 2 половых хромосом X и Y.
Строение половых желез определяет гонадный пол.
Яичники в эмбриональном периоде функционально неактивны, и дифференцировка по женскому типу идет пассивно, не требуя контроля со стороны половых желез. Семенник зародыша очень рано становится активным эндокринным органом. Под влиянием андрогенов, вырабатываемых эмбриональными яичками, происходят развитие и формирование внутренних и наружных половых органов по мужскому типу. Формируются и развиваются семявыносящие канальцы, придатки яичек, семенные пузырьки, предстательная железа; образуются мошонка, половой член, мочеиспускательный канал, происходит постепенное опускание яичек в мошонку. При отсутствии андрогенов, нарушении их выработки или нечувствительности периферических рецепторов к ним в процессе эмбриогенеза наружные половые органы могут формироваться по женскому типу или же развиваются различные их аномалии. С момента рождения пол определяется строением наружных половых органов, после чего закрепляется психоаффективной сексуализацией на первых 18-30 мес жизни ребенка и подкрепляется на протяжении всей дальнейшей жизни.
В период полового созревания яички активно продуцируют тестостерон, который способствует появлению вторичных половых признаков, и утверждают мужской гормональный пол. К этому времени оформляется и гражданский пол, характеризующийся внешними признаками пола, одеждой, манерой, социальным поведением, ориентацией полового влечения.
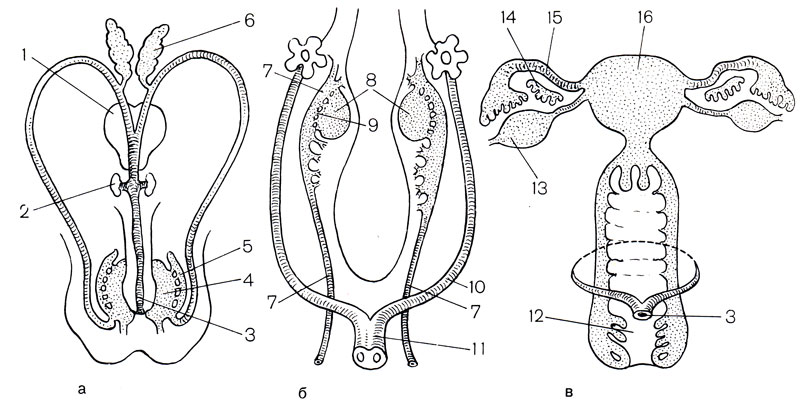
Рис. 7. Схема половой дифференцировки эмбриона, а - мужской эмбрион после 11 нед; б - 6-недельный эмбрион (недифференцированный); в - женский эмбрион после 11 нед. 1 - предстательная железа; 2 - Куперовы железы; 3 - уретра; 4 - яичко; 5 - придаток яичка; 6 - семенные пузырьки; 7 - вольфов канал; 8 - первичная половая железа; 9 - вольфово тело; 10 - мюллеров канал; 11 -слившийся мюллеров канал; 12 - влагалище; 13 - яичник; 14 - гартнеров тяж; 15 - маточная труба; 16 - матка
Развитие половых желез. Половые органы тесно связаны с мочевыми и формируются из первичной почки зародыша - mesonephros. За счет разрастания многослойного эпителиального покрова, покрывающего mesonephros, образуется зародышевый валик - эпителиальный зачаток первичной половой железы. Он проникает в глубину mesonephros, образуя первичные половые тяжи, состоящие из первичных половых клеток - гоноцитов (предшественников спермиев), соединительнотканных клеток, которые будут секретировать половые гормоны, а также недифференцированных клеток, исполняющих трофическую и опорную роль. С 7-й недели тканевые структуры первичной половой железы плода начинают дифференцироваться в мужские (семенники) или женские (яичники) половые железы. При развитии семенника с 8-й недели первичные половые тяжи активно разрастаются и превращаются в семенные канальцы с образованием в них просветов. В просвете семенных канальцев находятся половые клетки - сперматогонии, которые образуются из гоноцитов и в будущем положат начало сперматогенезу. Сперматогонии располагаются на сустентоцитах, осуществляющих трофическую функцию. Из соединительнотканных зачатков mesonephros образуются межуточные клетки, способные вырабатывать мужские половые гормоны в течение определенного периода эмбриогенеза. Развитие первичной половой железы в семенники завершается к 60-му дню внутриматочного развития плода. Установлено, что плодным яичком выделяются андростандион, андростерон и прочие стероиды андрогенной природы. Выделение тестостерона более выражено на 9-15-й неделе. Уже на 10-й неделе развития уровень тестостерона в семенниках плода человека в 4 раза выше, чем в яичниках. На 13-15-й неделе эмбрионального развития уровень тестостерона в семенниках превышает содержание его в яичнике в 1000 раз. От продукции тестостерона зависит дальнейшее формирование внутренних и внешних половых органов.
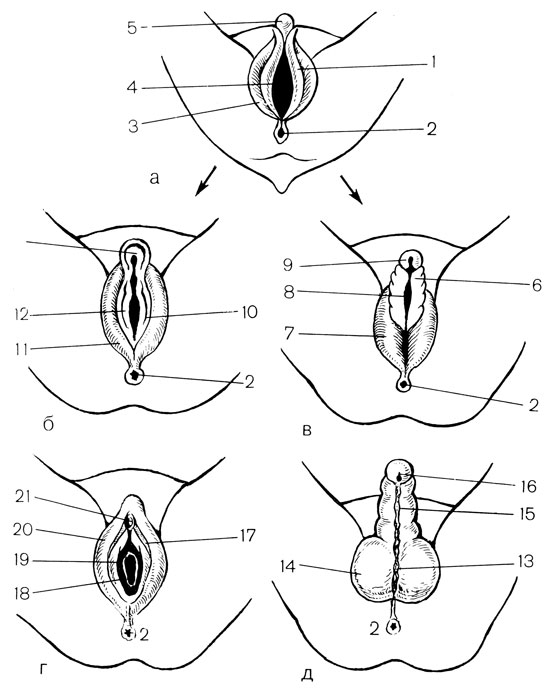
Рис. 8. Схема дифференцировки наружных половых органов плода (слева - девочка, справа - мальчик). а - 2-3 мес; б-в - 3-4 мес; г-д - в момент рождения; f - половая складка; 2 - анус; 3 - половой валик; 4 - половая щель; 5 - половой бугорок; 6 - уретральная складка; 7 - мошоночный валик; 8 - уретральная щель; 9 - половой отросток; 10 - складка внутренней половой губы; 11 - валик наружной половой губы; 12 - вульварная щель; 13 - шов мошонки; 14 - мошонка; 15 - уретральный шов; 16 - половой член; 17 - малая половая губа; 18 - вход во влагалище; 19 - отверстие уретры; 20 - большая половая губа; 21 - клитор
Развитие внутренних половых органов. С развитием тазовой почки у высших позвоночных первичная почка теряет свое назначение выделительного органа. В конце 2-го месяца внутриутробного периода выводной канал первичной почки расщепляется на 2 протока: ductus mesoenphricus (вольфов проток) и ductus paramesonephricus (мюллеров проток) (рис. 7). Из ducti mesonephrici развиваются семявыносящие пути, из ducti paramesonephrici формируется маточная труба. Мужские половые гормоны, выделяемые эмбриональными семенниками, способствуют обособлению и развитию ducti mesonephrici. Кроме того, яички секретируют еще какие-то другие факторы нестероидной природы, под влиянием которых происходят регресс и атрофия мюллеровых каналов. Верхний отдел ducti mesonephrici (после обратного развития первичной плоти) соединяется с семенными канальцами яичка и образует семявыносящие канальцы, сеть яичка, канал придатка яичка. Средняя часть ducti mesonephrici преобразуется в семявыносящий проток. Нижний отдел ducti mesonephrici (примыкающий к мочеполовому синусу) ампуловидно расширяется, образует выпячивание, из которого формируется семенной пузырек. Самая нижняя часть ducti mesonephrici, открывающаяся в мочеполовой синус, превращается в семявыбрасывающий проток. Тазовая часть мочеполового синуса трансформируется в предстательную и мембранозную части мочеиспускательного канала и дает зачатки предстательной железы, врастая в окружающаю мезенхиму в виде сплошных тяжей. Из мезенхимы развиваются мышечные и соединительнотканные элементы железы. Просветы в предстательной железе появляются после рождения, к периоду полового созревания.
Ductus paramesonephricus при развитии мужского организма исчезают, остаются только их рудименты: верхняя часть - отросток яичка и самая нижняя часть, из которой образуется мужская маточка - слепой придаток предстательной части уретры на семенном бугорке.
Развитие наружных половых органов. Наружные половые органы у обоих полов формируются из полового бугорка и клоакальной щели. Общая клоака еще на ранних стадиях развития зародыша разделяется спускающейся сверху перегородкой на 2 отдела: задний (задний проход) и передний (мочеполовая щель, в которую выходят вольфовы и мюллеровы протоки). Из мочеполовой щели формируются мочевой пузырь и мочеиспускательный канал, а также мочеточники и почечные лоханки. На нейтральной стадии наружные половые органы представлены половым бугорком мочеполовой щели и двумя парами складок, охватывающих ее (рис. 8.). Внутренние называются половыми складками, внешние - половыми валиками. С 4-го месяца эмбриональной жизни начинается дифференцировка наружных половых органов. У мужского зародыша под действием выделяемых семенником андрогенов половой бугорок растет, и из него развиваются головка, а позднее - пещеристые тела полового члена. Половые складки, окружая мочеполовое отверстие, распространяются на нижнюю часть полового бугорка, образуют уретральную бороздку. Края половых складок, срастаясь вдоль уретральной бороздки, формируют мочеиспускательный канал, вокруг которого из мезенхимы полового бугорка формируется пещеристое тело уретры. Половые валики у мужчин, соединяясь по всей протяженности, образуют кожную часть мошонки. В нее к моменту рождения плода опускаются яички. Хромосомные нарушения (количественные, структурные, генные мутации), эмбриотоксические воздействия эндогенного и экзогенного характера могут привести к развитию аномалий внутренних и наружных половых органов. Аномалии развития яичек включают аномалии положения, а также количественные и структурные.
Пороки развития
Аномалии положения яичек (крипторхизм)
Яички в процессе эмбриогенеза закладываются вместе с первичной почкой, и к концу 3-го месяца они мигрируют в подвздошную область. При смещении яичко вдается в брюшную полость, отодвигая перед собой брюшину, которая образует 2 складки. Краниальная складка брюшины покрывает сосуды и нервы, питающие яичко. Каудальная складка образует влагалищный отросток брюшины и покрывает задним своим листком направительный тяж, который состоит в основном из гладкомышечных волокон. К концу 7-го месяца яичко подходит к внутреннему кольцу пахового канала, куда до этого проникает направительный тяж. Активную роль в перемещении яичка в мошонку играют сократительная способность направительного тяжа, напряжение мышц живота, повышение внутрибрюшинного давления. На 8-м месяце яичко проходит паховый канал, при этом просвет влагалищного отростка брюшины широко сообщается с брюшной полостью. На 9-м месяце яичко опускается в мошонку. Направительный тяж редуцируется, превращаясь в связку, соединяющую каудальный полюс яичка с дном мошонки. Влагалищный отросток брюшины облитерируется в проксимальном отделе, и брюшная полость отграничивается от межоболочечного синуса яичка.
Отсутствие одного или обоих яичек в мошонке называется крипторхизмом (от греч. χριπτοζ - скрытый и 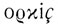 - яичко). Крипторхизм определяется у 10-20% новорожденных, у 2-3% годовалых детей, у 1% в пубертатном периоде и лишь у 0,2-0,3% взрослых мужчин. Такая статистика обусловлена тем, что незавершенное опущение яичка у новорожденных в большинстве наблюдений ликвидируется в первые недели внеутробного развития. До 1 года самостоятельное опущение яичка отмечается еще у 70% детей с крипторхизмом. В дальнейшем возможность самостоятельного смещения яичек в мошонку существует до периода половой зрелости.
- яичко). Крипторхизм определяется у 10-20% новорожденных, у 2-3% годовалых детей, у 1% в пубертатном периоде и лишь у 0,2-0,3% взрослых мужчин. Такая статистика обусловлена тем, что незавершенное опущение яичка у новорожденных в большинстве наблюдений ликвидируется в первые недели внеутробного развития. До 1 года самостоятельное опущение яичка отмечается еще у 70% детей с крипторхизмом. В дальнейшем возможность самостоятельного смещения яичек в мошонку существует до периода половой зрелости.
Этиология и патогенез. Задержка миграции яичек в мошонку может быть обусловлена эндокринными нарушениями, механическими причинами, дисгенезией половых желез, наследственно-генетическими моментами и сочетанием указанных факторов. В возникновении крипторхизма важная роль отводится эндокринному фактору. Гормональные дискорреляции у беременных женщин, нарушение инкреторной функции яичек, щитовидной железы, гипофиза эмбриона способны вызвать задержку перемещения яичек в мошонку. Указанные причины имеют значение при двустороннем крипторхизме.
При односторонней задержке яичка определенную роль играют механические факторы, среди которых во время операции выявляются: узость пахового канала; отсутствие туннеля в мошонку; укорочение семенного канатика, влагалищного отростка брюшины, сосудов, питающих яичко; недоразвитие направляющей связки; перитонеальные сращения в области внутреннего отверстия пахового канала и др. Перечисленные изменения могут возникать вследствие перенесенных заболеваний, травм во время беременности, но могут носить и вторичный характер на фоне гормональных нарушений во внутриутробном периоде развития плода.
Двусторонний брюшной крипторхизм нередко сочетается с дисгенезией яичек. Гистологическими исследованиями почти в половине наблюдений устанавливается первичная гипоплазия неопустившихся яичек. Поэтому у части больных, несмотря на раннее низведение в мошонку, яички остаются неполноценными. Вполне вероятно, что неправильно сформированное в эмбриональном периоде яичко предрасполагает к развитию крипторхизма вследствие нарушения инкреторной функции. В пользу дисгенезии яичек свидетельствует и большое количество аномалий придатка и семявыносящего протока, которые обнаруживаются при крипторхизме.
В ряде случаев неопущение яичек имеет наследственно-генетическую природу. Наблюдается семейный крипторхизм у мужчин нескольких поколений. Врачи, которые лечат крипторхизм, должны обращать внимание на изучение семей больных мальчиков.
Классификация. До настоящего времени нет общепринятой классификации крипторхизма. Наиболее соответствует правильному толкованию терминологии этого заболевания классификация С. Л. Горелика, Ю. Д. Мирлеса (1968). Мы пользуемся своей классификацией крипторхизма и считаем ее удобной для применения в практической работе.
Крипторхизм может быть односторонним и двусторонним. Выделяются 4 вида крипторхизма: обусловленный ретенцией, эктопией, а также ложный и приобретенный.
Крипторхизм, обусловленный ретенцией (задержкой) яичка. Ретенция может быть брюшная, паховая, комбинированная. При брюшной ретенции одно или оба яичка могут располагаться в поясничной или подвздошной области; при паховой - в паховом канале. При комбинированной ретенции яичко с одной стороны обнаруживается в паховом канале, а с другой стороны находится в брюшной полости.
Крипторхизм, обусловленный эктопией (необычным местом расположения опустившегося яичка). Эктопия бывает промежностная, лобковая, бедренная, пенальная, поперечная и др. Эктопия возникает вследствие отклонения яичка от обычного пути следования в мошонку. При этом яичко может располагаться на лобке, промежности, внутренней поверхности бедра, у основания полового члена. При поперечной эктопии оба яичка находятся в одной из половин мошонки.
Ложный крипторхизм (так называемое мигрирующее яичко). Яичко может временно под действием холода или физических нагрузок мигрировать в паховый канал и даже в брюшную полость. При согревании и расслаблении мышц оно возвращается в мошонку. При ложном крипторхизме мошонка всегда хорошо развита, с выраженной складчатостью и заметным серединным швом, паховое кольцо несколько расширено.
Приобретенный крипторхизм. Чаще всего после травмы яичко может уйти в брюшную полость или паховый канал. К этому предрасположено мигрирующее яичко, при котором паховый канал достаточно широк. В других случаях миграции яичка в брюшную полость способствует его атрофия".
Диагностика крипторхизма основывается на анализе жалоб и осмотре больного. Основными симптомами являются недоразвитие, асимметрия мошонки, отсутствие одного или обоих яичек в мошонке. Часто больные жалуются на ноющие боли в паховой области или в животе. При крипторхизме, обусловленном паховой ретенцией или эктопией, боли появляются уже в раннем детстве из-за частого травмирования, ущемления, перекрута яичка. При брюшной задержке яичка боль, как правило, присоединяется лишь в периоде полового созревания. Она может усиливаться при физической нагрузке, задержке стула, половом возбуждении. У многих больных наблюдается сочетание крипторхизма с паховой грыжей. Поэтому пациентов нужно осматривать лежа, стоя, в спокойном состоянии и при напряжении брюшного пресса. При натуживании в паховый канал может опускаться грыжевой мешок вместе с яичком, которое становится доступным для исследования. Если в паховом канале прощупать яичко не удается, то следует тщательно осмотреть и пропальпировать места возможной эктопии. Только при исключении необычной локализации яичка можно заподозрить наличие брюшной ретенции. У 5-10% больных, особенно при двустороннем крипторхизме, могут наблюдаться признаки эндокринной недостаточности (евнухоидное телосложение, ожирение, недоразвитие полового члена, оволосение по женскому типу, гинекомастия). Однако эти симптомы более характерны для анорхизма. У некоторых больных отмечается задержка полового развития. Брюшную двустороннюю задержку яичек следует дифференцировать от анорхизма, а одностороннюю - от монорхизма, что нередко довольно трудно. В настоящее время для этого с успехом применяется ядерно-магнитный резонанс, ультразвуковое сканирование, а также сцинтиграфия яичек после введения соединений 99mmТс. При сцинтиграфии с помощью гамма-камеры удается определить не только локализацию и размеры яичка, но и его функциональное состояние. Ценную информацию может дать ангиография: исследование брюшной аорты для обнаружения яичковой артерии, а также суперселективное зондирование внутренней яичковой вены с выполнением венографии неопустившегося яичка. В сомнительных случаях показана оперативная ревизия паховой области и забрюшинного пространства.
При различных видах крипторхизма на яичко, расположенное в необычных для него условиях, действует ряд неблагоприятных факторов: повышенная температура, постоянная травматизация, нарушение питания, а также гиперстимуляция со стороны гипофиза. Эти условия приводят к развитию атрофических процессов в яичке, к нарушению сперматогенеза и могут вызвать его злокачественное перерождение. При крипторхизме могут также наблюдаться ущемление или перекрут яичка. Признаками этих осложнений служат внезапное появление болей в ретенированном или эктопированном яичке, припухлость, в редких случаях - повышение температуры тела. При подозрении на перекрут или ущемление для предупреждения некротических изменений в яичке необходимо срочное оперативное вмешательство.
Лечение крипторхизма может быть консервативным, оперативным и комбинированным. Консервативное лечение должно быть направлено на улучшение функционального состояния яичка и на коррекцию эндокринных нарушений, которые нередко сопутствуют крипторхизму. Терапия может проводиться во всех случаях как предоперационная подготовка у больных с гормональными нарушениями, а также может иметь место в послеоперационном периоде.
Лечение начинают с 4-5-летнего возраста. Широко используют витаминные препараты. Токоферола ацетат (витамин Е) регулирует гистобиохимические процессы в клетках Лейдига и в эпителии канальцев яичка путем стимуляции гипоталамо-гипофизарной системы. Ретинол (витамин А) активизирует процессы клеточной регенерации в яичках, а также участвует в формировании ядерных структур сперматогенного эпителия. Витамины С, Р, B1 улучшают окислительно-восстановительные процессы в тканях, имеют большое значение для нормального функционирования эндокринных желез центральной и периферической нервной системы.
И. Ф. Юнда (1981) рекомендует начинать лечение истинного крипторхизма сразу же после рождения ребенка назначением кормящей матери токоферола ацетата внутримышечно по 200-300 мг/сут. В возрасте старше 1 мес ребенку дают токоферола ацетат в микстуре по 5-10 мг/сут в 2-3 приема в течение 1 ½ - 2 мес. С месячным перерывом курс лечения повторяют 3-4 раза в год. Кормящей матери назначают поливитамины. Важное значение должно придаваться полноценному питанию ребенка. Пища должна содержать достаточное количество белков, жиров и углеводов. При пониженном питании можно провести лечение нероболилом, который относится к анаболическим стероидам, стимулирует синтез белка в организме, улучшает обменные процессы в придаточных половых железах. При избыточном питании, ожирении рекомендуется применять тиреоидин, который повышает тканевое дыхание, улучшает обмен веществ в организме, активирует антитоксическую функцию печени, выделительную способность почек, нормализует функции щитовидной и половых желез.
Указанные препараты назначают в зависимости от возраста, индивидуальных особенностей и состояния пациента. Тиреоидин в таблетках рекомендуют по 0,005 г в возрасте 5 лет, 0,05 г - в возрасте 15 лет 1-2 раза в день в течение 15-25 дней. Нероболил в таблетках назначают: от 3 мг 1 раз в день в возрасте 5 лет, до 5 мг 1 -2 раза в день в возрасте 15 лет (в течение 20-30 дней).
Ретенированное яичко отличается пониженной способностью к выработке тестостерона, что при двустороннем, а нередко и при одностороннем процессе сопровождается гипоандрогенемией. Для стимуляции функции интерстициальных клеток яичка проводится терапия хорионическим гонадотропином, содержащим преимущественно Л Г. Увеличение выработки тестостерона межуточными клетками может способствовать опущению ретенированного яичка. В зависимости от возраста вводят внутримышечно 250, 500 или 1000 ЕД хорионического гонадотропина (хориогонина) от 1 до 3 раз в неделю, на курс лечения 6-18 инъекций. М. Г. Георгиева (1969) рекомендует вводить хориогонин по 500-700 ЕД 1 раз в день в течение 3 дней в паховый канал со стороны неопущенного яичка, что оказывает, кроме обычного, местное депрессорно-лизирующее действие. При выраженной андрогенной недостаточности возможно сочетанное применение нероболила (неробола) и хориогонина в дозах, соответствующих возрасту. В период полового созревания при явных признаках гипогонадизма целесообразно назначать внутримышечные инъекции тестостерона по 10-20 мг через день (на курс 15-20 инъекций). После этого проводится лечение хориогонином по 1000 ЕД внутримышечно 3 раза в неделю (на курс 12 инъекций).
Основным методом лечения крипторхизма остается оперативный (орхипексия). Мы считаем, что орхипексию целесообразно проводить в возрасте 5-6 лет, к моменту поступления ребенка в школу. Более раннее оперативное лечение, очевидно, не имеет смысла, так как в этом возрасте еще не сформированы сосудистая система и семенной канатик.
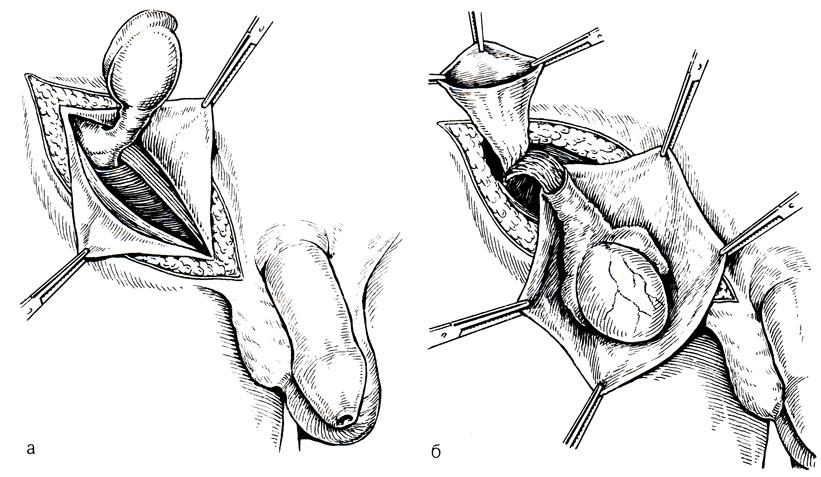
Рис. 9. Мобилизация семенного канатика и яичка единым блоком вместе с влагалищным отростком брюшины; (а) мобилизация семенного канатика выделением влагалищного отростка брюшины и грыжевого мешка (б)
Существует большое количество способов низведения яичек в мошонку. Но все они различаются в конечном счете лишь методами фиксации.
Операцию проводят под наркозом. Разрез производят в паховой области, как при грыжесечении. После вскрытия передней стенки пахового канала отыскивают яичко. Основным методом низведения яичка в мошонку является мобилизация семенного канатика (рис. 9, а). При этом следует обязательно отделить от него незаращенный влагалищный отросток брюшины (рис. 9, б). При наличии грыжи влагалищный отросток превращается в грыжевой мешок. В таком случае его следует вскрыть, затем с помощью гидравлической препаровки рассечь в поперечном направлении брюшину, покрывающую семенной канатик, и, снимая ее с семенного канатика, выделить, прошить и перевязать шейку грыжевого мешка. После этого следует пальцем проникнуть во внутреннее кольцо пахового канала, тупо расшить его в медиальном направлении и отделить брюшину от семенного канатика. Тщательное отделение грыжевого мешка и брюшины от семенного канатика в большинстве случаев способствует низведению яичка в мошонку. Следует критически относится к рекомендациям пересекать яичковую артерию для удлинения семенного канатика, так как это может привести к атрофии яичка из-за нарушения питания. Однако при короткой сосудистой ножке возможна аутотрансплантация яичка в мошонку с использованием для артериализации его нижнюю надчревную артерию или же, что менее благоприятно, пересадка яичка на подвздошные сосуды. В соответствующей половине мошонки, раздвигая ткани, создают ложе для яичка. У взрослых чаще фиксируют яичко в мошонке толстой шелковой лигатурой, прошитой за мобилизованные оболочки яичка, выведенной через дно мошонки и прикрепленной посредством эластической резиновой тяги к специальной манжетке, надетой на верхнюю треть голени. Операцию заканчивают пластикой пахового канала по способу Мартынова или Кимбаровского.
У детей орхипексию можно выполнять в 2 этапа методом Торека - Герцена и его модификациями. После мобилизации семенного канатика яичко проводят в соответствующую половину мошонки. Через разрез в дне мошонки и кожи бедра яичко подводят и подшивают к широкой фасции бедра. Затем над яичком сшивают края разрезов мошонки и кожи бедра. Ногу укладывают на шину Белера.
Больных выписывают на 10-12-й день после операции. Второй этап операции производится через 2-3 мес. Он заключается в иссечении кожного анастомоза и зашивании небольших ран на бедре и мошонке.
Операция при эктопии бывает достаточно проста вледствие значительной длины семенного канатика. Поперечная эктопия яичка лечения не требует.
При двусторонней ретенции вопрос решается индивидуально с учетом жалоб больного и сохранности одного из яичек. Предпочтение следует отдавать раздельному низведению яичек. При этом мы начинаем с менее сложного оперативного вмешательства.
Прогноз при крипторхизме, обусловленном ретенцией яичек, улучшается после оперативного лечения. Бесплодие излечивается у 80% оперированных при одностороннем и у 30% - при двустороннем крипторхизме.
Аномалии количества и структуры яичек
Причиной нарушения нормального хода эмбриогенеза половых желез могут быть хромосомные аномалии (структурные или количественные), нарушения хода дифференцировки половых желез на ранних этапах эмбрионального развития вследствие тяжелых инфекционных заболеваний, интоксикаций, алиментарной дистрофии или гормональных сдвигов у беременной. Чисто количественные аномалии яичек встречаются крайне редко, в большинстве случаев они сочетаются с их структурными изменениями.
Полиорхизм. Наличие более 2 яичек является редкой аномалией. Описано 36 случаев полиорхизма [Butz R., Croushor J., 1978]. Добавочное яичко может иметь свой придаток и семявыносящий проток. Яичко и придаток обычно недоразвиты. Пальпации недостаточно для подтверждения наличия дополнительного яичка, так как опухоли яичка, добавочные придатки, кисты и другие внутримошоночные образования могут быть ошибочно приняты за дополнительное яичко. Удвоенные яички могут располагаться в брюшной полости и подвергаться дегенеративным изменениям.
Учитывая склонность гипоплазированных яичек к злокачественному перерождению, показано оперативное удаление добавочного яичка с низведением нормального при наличии крипторхизма.
Синорхидизм. Крайне редко наблюдается внутрибрюшное сращение яичек, что препятствует их опущению в мошонку. Гормональных нарушений при этом не выявляется, что отличает данное патологическое состояние от анорхизма и двусторонней брюшной ретенции яичек. Диагностика основана на сканировании и оперативной ревизии забрюшинного пространства.
Монорхизм (односторонняя агенезия яичка) - врожденная аномалия, характеризующаяся наличием одного яичка. Данная аномалия возникает в результате нарушения эмбриональной закладки первичной почки с одной стороны, из которой образуется половая железа, поэтому монорхизм нередко сочетается с врожденной аплазией почки, отсутствием придатка и семявыносящего протока, наблюдается недоразвитие мошонки на соответствующей стороне. Наличие одного нормального яичка не проявляется расстройствами сперматогенеза и эндокринными нарушениями. Если же единственное яичко не опускается в мошонку или находится в рудиментарном состоянии, то наблюдаются признаки гипогонадизма.
Диагноз может быть установлен с помощью ангиографии, сцинтиграфии яичек или при ревизии забрюшинного пространства и брюшной полости.
Лечение. При гипоплазии единственного яичка показана заместительная терапия андрогенами, особенно в период полового созревания. Такая терапия будет способствовать нормальному развитию половых органов.
Анорхизм (гонадная агенезия) - врожденное отсутствие яичек у индивида с кариотипом 46 XY. В связи с тем, что яички в эмбриональном периоде не секретируют андрогены, половые органы развиваются по женскому типу или имеют рудиментарное строение. Гораздо реже при этом наружные половые органы развиваются по мужскому типу. В таком случае отмечаются евнухоидное телосложение, отсутствие придатков яичка, семявыносящих протоков, предстательной железы; мошонка рудиментарная.
Окончательный диагноз ставится после исключения двусторонней брюшной ретенции яичек. Для этого могут быть произведены радионуклидные исследования и сцинтиграфия яичек после введения соединений 99mTc. После внутривенного введения препарата на γ-камере определяют локализацию и характер крипторхизма. При анорхизме локального накопления препарата не будет. Можно провести пробу с хориогонином на наличие тестикулярных андрогенов в крови. В сомнительных случаях показана оперативная ревизия брюшной полости и забрюшинного пространства.
Лечение. При анорхизме проводится заместительная терапия половыми гормонами в зависимости от строения наружных половых органов и морфотипа больного. Терапия андрогенными препаратами включает назначение метилтестостерона в таблетках по 5 мг 3 раза в день под язык или тестостерона пропионата по 50 мг (1 мл 5% масляного раствора) внутримышечно ежедневно. В дальнейшем можно применять препараты пролонгированного действия: сустанон-250; омнадрен-250, тестенат. Все они вводятся внутримышечно по 1 мл 1 раз в 2-3 нед. Применяется трансплантация половозрелых яичек на сосудистой ножке, а также свободная пересадка яичек плодов и новорожденных.
Феминизирующая терапия проводится в период полового созревания. При резком недоразвитии вторичных половых признаков назначают 0,1% масляный раствор эстрадиола дипропионата по 1 мл внутримышечно 1 раз в 7-10 дней. Лечение длится 3-4 мес для стимуляции вторичных половых признаков, после чего переходят на циклическую терапию. Назначают эстрадиола дипропионат по 1 мл 0,1% масляного раствора 1 раз в 3 дня, 5-7 внутримышечных инъекций. Вместе с последней инъекцией вводят прогестерон (1 мл 1% масляного раствора) и затем продолжают вводить его 7 дней подряд внутримышечно. Такие курсы циклической терапии повторяют 4-6 раз.
Гермафродитизм (двуполость) проявляется наличием у одного индивидуума признаков обоего пола. Различают истинный и ложный гермафродитизм. При истинном гермафродитизме в половых железах развиваются элементы как яичковой, так и яичниковой ткани. Половая железа может быть смешанной (овотестис), или, наряду с яичником (чаще слева), с другой стороны существует яичко. Нарушение дифференциации половых желез обусловлено хромосомными мозаиками XX/XY; XX/XXY; XX/XXYY и др., но встречаются также при кариотипе 46ХХ и 46XY. Гонадная ткань развивается неодинаково. На той стороне, где преимущественно развивается яичниковая ткань, сохраняются производные ducti paramesonephrici (матка, труба). На стороне, где формируется яичко, сохраняются производные ducti mesonephrici (семявыносящий проток, придаток яичка). Наружные половые органы имеют двойственное строение с преобладанием мужских или женских половых признаков. Морфотип больных определяется превалированием гормональной активности одной из половых желез в период полового созревания. Половой член развит при наличии гипоспадии, под ним располагается недоразвитое влагалище. Нередко наблюдаются циклические выделения крови из влагалища или мочеполового синуса. Развиваются молочные железы. Психический пол больных определяется чаще воспитанием, а не строением наружных половых органов. В зависимости от строения внутренних и наружных половых органов проводится корригирующее оперативное лечение, а также терапия женскими или мужскими половыми гормонами.
Ложный мужской гермафродитизм отмечается у индивидов с кариотипом 46XY, у которых при наличии яичек наружные половые органы развиваются по женскому или интерсексуальному типу. Причинами ложного мужского гермафродитизма могут быть гормональные сдвиги во время беременности, токсоплазмоз, интоксикации.
К этой аномалии яичек приводит также ряд генетически обусловленных заболеваний, из которых наиболее известен синдром феминизирующих яичек.
Синдром феминизирующих яичек. Эта аномалия развивается у лиц с мужским кариотипом 46XY и женским фенотипом. Она обусловлена нечувствительностью периферических тканей к андрогенам. Наружные половые органы развиты по женскому типу. У больных отсутствуют матка, маточные трубы, влагалище недоразвито, оканчивается слепо. Молочные железы развиты хорошо. Семенники могут располагаться в толще больших половых губ, в паховых каналах, в брюшной полости. Семейный канальцы недоразвиты, межуточная ткань гиперплазирована. Яички продуцируют нормальное количество андрогенов и повышенное количество эстрогенов. Заболевание генетически обусловлено, передается здоровой женщиной, носительницей рецессивного гена, половине своих сыновей.
Лечение путем введения экзогенных андрогенов не вызывает вирилизации. Яички сохраняют, так как они являются источником эстрогенов. Проводят феминизирующую гормональную терапию (см. Анорхизм).
Синдром Клайнфелтера (дисгенезия семенных канальцев) описан в 1942 г. Заболевание обусловлено наличием не менее одной добавочной Х-хромосомы в комплексе половых хромосом. Основная форма кариотипа 47XXY установлена P. Jacobsu I. Strong в 1959 г. Наблюдаются и другие хромосомные варианты этого синдрома - XXXY, XXXXY, XXYY, а также мозаичные формы типа XY/XXY и др. Частота синдрома среди новорожденных мальчиков достигает 2,5:1000. Заболевание проявляется в период полового созревания у относительно нормальных мальчиков. Взрослые мужчины обращаются к врачу по поводу бесплодия.
Клиническая картина характеризуется недостаточным развитием вторичных половых признаков: высоким ростом, евнухоидным телосложением, маленькими яичками, нормально развитым или уменьшенным половым членом, скудным ростом волос на лице и оволосением на лобке по женскому типу. У 50% больных выявляется гинекомастия. Клиническое проявление андрогенной недостаточности объясняется нарушением рецепции тканями тестостерона. Иногда отмечается различная степень психического недоразвития (более отягощена у больных с большим числом X-хромосом). При исследовании эякулята выявляется азооспермия. Устанавливается наличие X-полового хроматина в ядрах клеток слизистой оболочки полости рта.
При биопсии яичек определяется аплазия сперматогенного эпителия с гиалинозом семенных канальцев и гиперплазией интерстициальных клеток. Гормональная картина характеризуется низким уровнем тестостерона и высокими показателями ФСГ и ЛГ в плазме крови.
Описан хроматинотрицательный вариант синдрома Клайнфелтера с кариотипом 47 XYY. Гораздо реже у больных наблюдается полисомия Y-хромосом с набором XYYY или XYYYY. Индивиды с таким набором хромосом отличаются высоким ростом, физической силой, психопатическим поведением с чертами агрессивности и легкой степенью умственной отсталости. Частота этого синдрома среди новорожденных мальчиков 1:1000. Мужчины с кариотипом 47XYY фертильны. Дети от них могут иметь нормальный кариотип или иногда гетероплоидный набор хромосом.
Лечение заключается в назначении тестостерона и других андрогенов, витаминотерапии. Однако заместительная терапия бывает недостаточно эффективной из-за нарушения рецепции андрогенов клетками-мишенями придаточных половых желез, половых органов и других тканей. Гинекомастия подлежит оперативному лечению, так как опасна милигнизация молочных желез.
В период полового созревания и позднее проводится лечение тестенатом, сустаноном-250 или омнодреном-250, которые вводятся внутримышечно по 1 мл через каждые 3-4 нед. Лечение направлено на развитие вторичных половых признаков, рост полового члена, поддержание и усиление либидо. Сперматогенез не восстанавливается.
Синдром Шерешевского - Тернера является вариантом чистой дисгенезии половых желез. Заболевание описано в 1925 г. Н. А. Шерешевским у женщин. В 1938 г. Тернер для характеристики этого синдрома предложил основные симптомы: инфантилизм, крыловидная шейная складка, вальгусная девиация локтевых и коленных суставов. Кроме того, синдром Шерешевского - Тернера проявляется низким ростом (широкий плечевой пояс, узкий таз, укорочение нижних конечностей с деформацией пальцев рук и ног). При этом заболевании выражен половой инфантилизм. Яичники у женщин недоразвиты, в них практически отсутствует фолликулярный эпителий, продукция эстрогенов находится на очень низком уровне. Это приводит к недоразвитию матки, влагалища, аменорее, бесплодию, отсутствию вторичных половых признаков.
Было установлено, что более половины женщин с этим синдромом имеют моносомию Х-хромосом, кариотип 45X0. Возникновение этой аномалии связывают с нарушением сперматогенеза или овогенеза у родителей. Наблюдаются мозаичные формы (X0/XX, X0/XY). Реже фенотипический синдром Тернера определяется у мужчин с кариотипом 46XY. Этиология заболевания в таком случае объясняется наличием транслокации части Х-хромосом на Y-хромосому. Иногда выявляется мозаика X0/XY. Синдром Тернера проявляется у мужчин низким ростом и указанными изменениями тела, а также анатомическим и функциональным гипогонадизмом (гипотрофией половых органов, двусторонним крипторхизмом, низкой выработкой тестостерона, гипоплазированными яичками).
Лечение заключается в проведении феминизирующей терапии женщинам и назначении андрогенов мужчинам. Для стимулирования роста больных и развития наружных половых органов можно проводить лечение анаболическими гормонами и витаминотерапию.
Синдром Дель - Кастилло (терминальная агенезия). Этиология заболевания изучена недостаточно. Заболевание проявляется у взрослых мужчин с нормально развитыми наружными половыми органами и выраженными вторичными половыми признаками. Основной жалобой является бесплодие. Яички у больных нормальных размеров или слегка уменьшены. Гинекомастия не выявляется.
При исследовании эякулята определяется аспермия, реже - азооспермия. При гистологическом изучении биопсийного материала яичка выявляется отсутствие сперматогенного эпителия в канальцах. Базальная мембрана их выстлана лишь клетками Сертоли. Межуточная ткань яичка при этом синдроме не страдает. Секреция половых гормонов снижена. Уровни гонадотропинов повышены. При генетических исследованиях у больных устанавливается нормальный кариотип 46XY.
Del Castillo и соавт. (1947) считали терминальную агенезию врожденным пороком. В дальнейшем аналогичные изменения в канальцах яичек (терминальная атрофия) определялись у больных после лучевого воздействия и в эксперименте на животных при применении цистостатических препаратов.
Прогнозе отношении восстановления сперматогенеза неблагоприятный.
Врожденная гипоплазия яичек. Этиология полностью не изучена. В основе ее лежит недоразвитие половых желез в эмбриональном периоде, при отсутствии цитогенетических отклонений, у больных с мужским кариотипом 46XY. Гипоплазия чаще диагностируется случайно, при обращении пациентов по поводу бесплодного брака. Характерными для всей этой группы больных являются уменьшенные размеры яичек, расположенных в мошонке, гипоплазия придатков яичек, полового члена, предстательной железы, недостаточное терминальное оволосение, сопровождающееся иногда диспропорциональным развитием частей тела, псевдогинекомастией. При исследовании биоптатов яичка выявляется различной степени гипоплазия сперматогенного эпителия в канальцах, спермин встречаются редко или совсем отсутствуют. В межуточной ткани отмечаются дегенерация и скопление клеток Лейдига. Секреция половых гормонов снижена при повышенном или пониженном уровне гонадотропинов.
Лечение заключается в проведении андрогенной терапии или назначении гонадотропинов, биогенных стимуляторов, витаминов А, Е и др.
Аномалии полового члена и мочеиспускательного канала
Гипоспадия - врожденное недоразвитие губчатой части уретры с замещением недостающего участка соединительной тканью и искривлением полового члена в сторону мошонки. Она является одной из наиболее часто встречающихся аномалий мочеиспускательного канала (у 1 из 150-300 новорожденных). Гипоспадия развивается вследствие задержки или нарушения формирования уретры на 10-14-й неделе эмбрионального развития. Причинами ее могут быть экзогенные интоксикации, внутриутробные инфекции, гиперэстрогения у матери во время формирования у плода половых органов и мочеиспускательного канала. В результате наружное отверстие мочеиспускательного канала открывается выше естественного и может располагаться в области венечной борозды, на вентральной поверхности полового члена, в области мошонки или промежности. В зависимости от локализации наружного отверстия уретры различают головчатую, стволовую, мошоночную и промежностную гипоспадию. При любой форме гипоспадии между наружным отверстием и головкой сохраняются узкая полоска слизистой оболочки и плотный фиброзный тяж (хорда). При этой форме аномалии мочеиспускательный канал становится короче кавернозных тел. Наличие укороченной уретры и короткой неэластичной хорды приводит к искривлению полового члена. Головка полового члена пригнута книзу, широкая, а препуциальный мешок имеет вид капюшона.
Клиническая картина. Жалобы больных зависят от их возраста и от вида гипоспадии. Если детей беспокоит главным образом расстройство мочеиспускания, то взрослых - затруднение или невозможность полового акта.
При головчатой гипоспадии, на которую приходится почти 70% всех гипоспадии, дети и взрослые жалоб почти не предъявляют. Мочеиспускательный канал при этом открывается у места обычного расположения уздечки, что не вызывает особых расстройств. Жалобы возникают лишь при наличии стеноза наружного отверстия или при слишком сильно наклоненной головке, когда моча попадает на ноги.
При стволовой гипоспадии деформация полового члена более выражена. Наружное отверстие располагается на задней поверхности полового члена между головкой и корнем мошонки. Во время мочеиспускания струя направлена книзу, что затрудняет опорожнение мочевого пузыря. Эрекция становится болезненной, а деформация полового члена нарушает половой акт.
При мошоночной гипоспадии половой член несколько уменьшен и напоминает клитор, а наружное отверстие уретры располагается в области расщепленной, напоминающей половые губы, мошонки. Больные при этом мочатся по женскому типу, моча разбрызгивается, что вызывает мацерацию внутренних поверхностей бедер. Новорожденных с мошоночной гипоспадией иногда ошибочно принимают за девочек или ложных гермафродитов.
При промежностной гипоспадии отверстие уретры располагается еще более кзади на промежности. Половой член также напоминает клитор, а расщепленная мошонка - половые губы. Промежностная гипоспадия часто сочетается с крипторхизмом, что еще больше затрудняет половую дифференциацию больных.
Дети рано начинают понимать свою неполноценность, становятся замкнутыми, раздражительными, уединяются. После окончания полового развития они жалуются на невозможность совершения полового акта.
Диагностика типичной гипоспадии особых трудностей не вызывает. Однако дифференцировать мошоночную и промежностную гипоспадию от женского ложного гермафродитизма подчас очень трудно. Необходимо обращать внимание на крайнюю плоть, которая у мальчиков с гипоспадией располагается на дорсальной поверхности полового члена. При ложном гермафродитизме она переходит на вентральную поверхность клитора и сливается с малыми половыми губами. Влагалище у этих больных хорошо сформировано, но иногда как дивертикул выходит из просвета уретры. Необходимо также исследовать содержание 17-КС в моче и выявлять мужской и женский хроматин. Из рентгенологических методов применяют генитографию (для обнаружения матки и придатков), уретрографию для выявления мочеполового синуса и оксигеносупраренографию. Значительные возможности имеет ядерно-магнитно-резонансная и ультразвуковая диагностика. В особо затруднительных случаях для выявления яичников производят лапароскопию или лапаротомию.
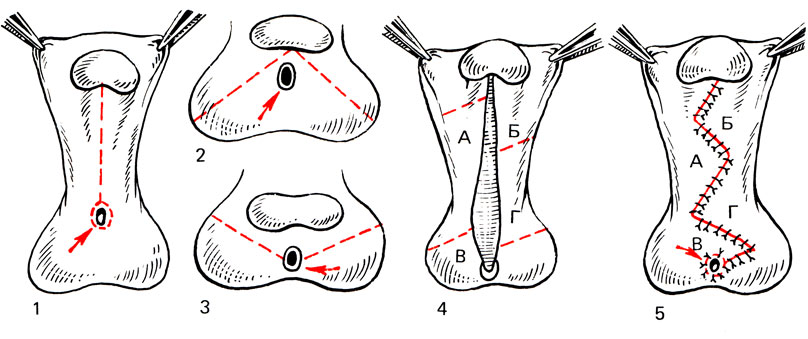
Рис. 10. Варианты операции выпрямления полового члена при гипоспадии (1-5)
Лечение. Головчатая гипоспадия и гипоспадия дистальной стволовой трети мочеиспускательного канала, если нет значительного искривления полового члена или стеноза, в хирургической коррекции не нуждается. В остальных случаях оперативное лечение является методом выбора.
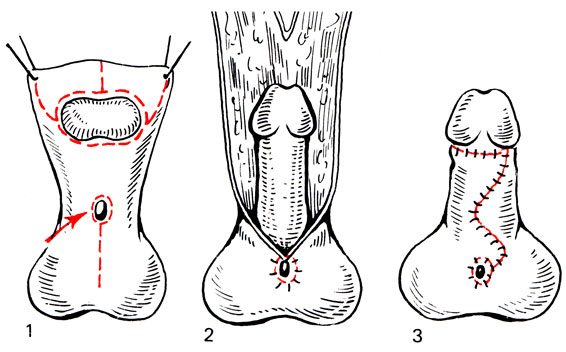
Рис. 11. Схема пластики кожного дефекта по Смиту - Блекфилду в модификации Савченко (1 - 3 - этапы операции)
К настоящему времени предложено много различных оперативных методов лечения, но общими для всех являются следующие рекомендации: производить операцию уже в первые годы жизни, т. е. еще до появления необратимых процессов в кавернозных телах; первый этап операции - выпрямление полового члена - осуществляют в возрасте 1-2 года; второй этап - создание недостающего отрезка уретры - в возрасте 6-13 лет.
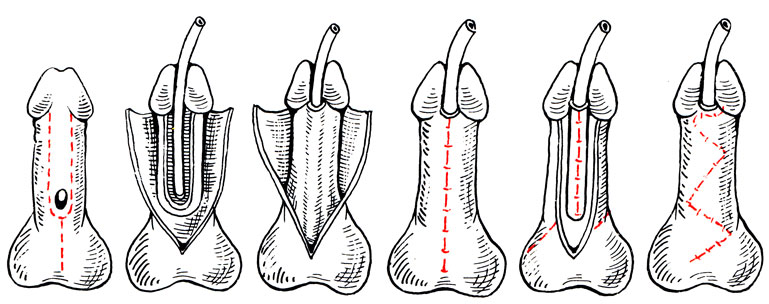
Рис. 12. Схема пластики по Дюплею в модификации Савченко
Первый этап заключается в тщательном иссечении хорды (рубцовых тканей на задней поверхности), фиброзной перегородки кавернозных тел, мобилизации полового члена из рубцов в мошонке и иссечении уздечки. Одновременно производятся выделение наружного отверстия уретры и перемещение его кверху. Для нормального развития кавернозных тел образовавшийся после выпрямления дефект полового члена подлежит закрытию кожным лоскутом. Применяется много различных методов закрытия дефекта кожи (мостовидные лоскуты кожи живота или бедра, перемещение кожи крайней плоти из верхней части головки полового члена на нижнюю, применение филатовского стебля и т. д.). Однако эти методы не получили широкого распространения. Чаще всего для замещения дефекта применяют так называемую унифицированную схему, когда используют кожу препуциального мешка и мошонки в виде мобильных треугольных лоскутов на широком питающем основании [Савченко H. Е., 1977] (рис. 10). Унификация позволяет мобилизовать и переместить запасы кожи крайней плоти и мошонки по методу Смита-Блекфилда в модификации H. Е. Савченко (рис. 11). Как правило, после операции наблюдаются смещение мочеиспускательного канала в проксимальном направлении и увеличение степени гипоспадии. Однако это не влияет на дальнейший ход операции. Половой член затем фиксируют на 8-10 дней к коже живота. Операция заканчивается отведением мочи через уретральный катетер.
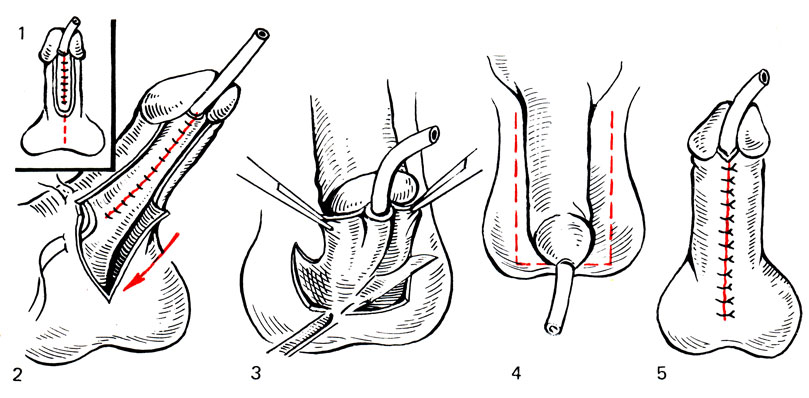
Рис. 13. Схема пластики мочеиспускательного канала по Сесилу - Калпу (1-5 этапы операции)
Второй этап операции производится не ранее чем через 6 мес после первого. Предложено около 50 различных способов формирования мочеиспускательного канала. Однако наиболее перспективными являются методы с использованием близлежащих тканей. Так, например, по Дюплею, на нижней поверхности полового члена от головки и вокруг отверстия уретры выкраивают кожный лоскут и формируют мочеиспускательный канал (рис. 12). Затем уретру погружают путем сшивания по средней линии оставшимися по бокам лоскутами. Если кожи недостаточно, то погрузить вновь созданную уретру можно встречными треугольными лоскутами. Если же дефект кожи носит тотальный характер на всем протяжении полового члена, то уретру можно временно погрузить в мошонку. После приживления на мошонке производят параллельные разрезы и выкраивают лоскуты для прикрытия вновь сформированного мочеиспускательного канала по Сесилу - Калпу (рис. 13). Методика операции в модификации Н. Е. Савченко позволяет унифицировать пластику мочеиспускательного канала при всех видах гипоспадии и является методом выбора. Во избежание эрекции всем больным после операции назначают транквилизаторы, валериану или бромиды (камфоры монобромид, натрия бромид).
Эписпадия - порок развития мочеиспускательного канала, для которого характерно недоразвитие или отсутствие на большем или меньшем протяжении верхней его стенки. Встречается реже, чем гипоспадия, примерно у 1 из 50000 новорожденных. У мальчиков различают эписпадию головки, эписпадию полового члена, тотальную эписпадию. Мочеиспускательный канал в этих случаях расположен на дорсальной поверхности полового члена между расщепленными пещеристыми телами. При любой форме эписпадии половой член в той или иной степени уплощается и укорачивается за счет подтянутости к передней брюшной стенке, а крайняя плоть сохраняется лишь на его вентральной поверхности. Причиной эписпадии является неправильное развитие мочеполового синуса, полового бугорка и урогенитальной мембраны. В результате смещения уретральной пластинки она оказывается над половым бугорком. Половые складки при формировании мочеиспускательного канала не срастаются, оставляя расщепленной его верхнюю стенку.
Клиническая картина. Симптоматика зависит от формы эписпадии.
Эписпадия головки полового члена характеризуется расщеплением спонгиозного тела головки по дорсальной поверхности, где у венечной борозды определяется наружное отверстие мочеиспускательного канала. Головка уплощена. При эрекции отмечается незначительное искривление полового члена кверху. Мочеиспускание не нарушено, отмечается лишь ненормальное направление струи мочи.
Эписпадия полового члена сопровождается уплощением, укорочением и искривлением его кверху. Головка и пещеристые тела расщеплены, по дорсальной поверхности свободны от крайней плоти, которая сохраняется лишь на вентральной стороне полового члена. Наружное отверстие в виде воронки открывается на теле полового члена или у корня его. От наружного отверстия до головки тянется уретральный желоб, выстланный полоской слизистой оболочки. Сфинктер мочевого пузыря сохранен, тем не менее нередко отмечается слабость его. Поэтому при напряжении брюшного пресса может наблюдаться недержание мочи. Значительное разбрызгивание мочи заставляет мочиться сидя, оттягивая половой член к промежности. У взрослых присоединяются жалобы на затруднение или невозможность совершения полового акта из-за деформации и искривления полового члена, усиливающихся во время эрекции.
Тотальная эписпадия характеризуется полным отсутствием передней стенки мочеиспускательного канала, расщеплением на всем протяжении пещеристых тел и сфинктера мочевого пузыря. Половой член недоразвит, изогнут кверху и подтянут к животу. Наружное отверстие мочеиспускательного канала в виде широкой воронки располагается у основания полового члена и ограничено сверху кожной складкой передней брюшной стенки. Из-за постоянного подтекания мочи имеется мацерация кожи промежности и бедер. При тотальной эписпадии наблюдается значительное расхождение костей лобкового симфиза, в связи с чем у больных отмечаются утиная походка и распластанный живот.
Заболевание сочетается с крипторхизмом, гипоплазией яичек, с недоразвитием мошонки, предстательной железы и пороками развития верхних мочевых путей. Тотальная эписпадия обусловливает наибольшую степень расстройств мочеиспускания и полностью лишает взрослых больных половой функции.
Диагностика эписпадии трудностей не вызывает и основывается на простом осмотре больных. Необходимо исследовать почки и верхние мочевые пути для исключения аномалии и пиелонефрита.
Лечение. Эписпадия головки в коррекции чаще всего не нуждается. В остальных случаях показано оперативное лечение, которое должно быть направлено на восстановление мочеиспускательного канала, шейки мочевого пузыря, коррекцию деформаций и искривления полового члена. Выбор метода операции должен производиться в зависимости от формы эписпадии и индивидуальных особенностей больного. Оперативная коррекция выполняется в возрасте 4-5 лет. Перед операцией необходимо устранить опрелости и мацерацию кожи.
Значительные трудности возникают при восстановлении сфинктера мочевого пузыря с последующей пластикой мочеиспускательного канала. Наибольшее распространение получили операции пластики шейки мочевого пузыря и уретры по Юнгу - Диссу и пластики шейки мочевого пузыря по Державину.
Операция Юнга - Дисса заключается в иссечении рубцовой ткани и формировании задней уретры и шейки мочевого пузыря за счет мочевого треугольника. Мочевой пузырь вскрывают разрезом от верхушки до наружного сфинктера. С боков выкраивают и иссекают 2 треугольных участка слизистой оболочки. Из оставшейся срединной дорожки слизистой оболочки формируют уретру. Демукузированные боковые лоскуты мобилизуют и сшивают внахлест, формируя шейку мочевого пузыря. Лобковые кости сближают капроновыми швами. Сформированную дистальную часть мочеиспускательного канала погружают, сшивая над ней пещеристые тела за белочную оболочку и кожу полового члена (рис. 14). Для отведения мочи используют эпицистостому.
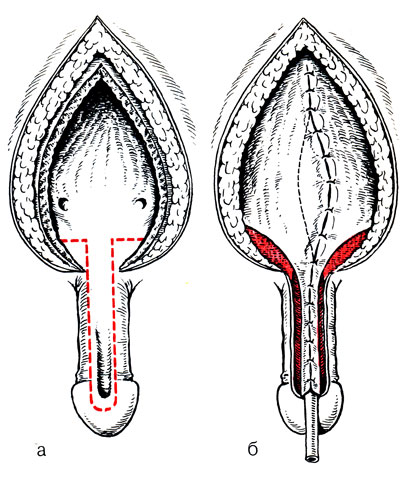
Рис. 14. Пластика шейки мочевого пузыря и уретры по Юнгу - Диссу при полной эписпадии. а - мочевой пузырь вскрыт по средней линии, выкроены и иссечены треугольные лоскуты слизи стой оболочки (заштрихованы); б - мобилизованные стенки мочевого пузыря сшиты внахлест; из срединной пластинки сформирована на катетере уретра
Операция Державина заключается в формировании сфинктера мочевого пузыря без рассечения стенки за счет продольного гофрирования шейки и стенки его. Продольным чрезлобковым рассечением тканей обнажают переднюю стенку мочевого пузыря. Затем на катетере двумя рядами погружных швов инвагинируют каждый раз продольную полоску мочевого пузыря шириной около 3 см на протяжении 6-7 см (рис. 15). Добившись плотного охвата катетера ушитыми тканями, дренируют паравезикальное пространство, послойно ушивая рану. Катетер оставляют на 12-14 дней для дренирования мочевого пузыря.
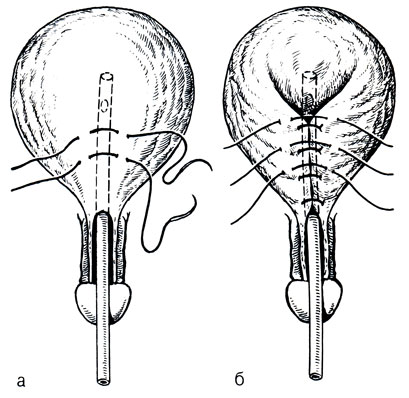
Рис. 15. Пластика шейки мочевого пузыря при полной эписпадии по Державину, а - наложение первого ряда швов, сужающих шейку мочевого пузыря; б - наложение второго ряда швов. а - мочевой пузырь вскрыт по средней линии, выкроены и иссечены треугольные лоскуты слизи стой оболочки (заштрихованы); б - мобилизованные стенки мочевого пузыря сшиты внахлест; из срединной пластинки сформирована на катетере уретра
Пластика мочеиспускательного канала применяется как самостоятельная операция при эписпадии головки или полового члена, она может также являться завершающим этапом в лечении тотальной эписпадии. Различные методы формирования мочеиспускательного канала при эписпадии отличаются друг от друга степенью мобилизации слизистой оболочки при создании уретральной трубки, а также перемещением ее на вентральную поверхность или оставлением на тыльной поверхности полового члена.
Операция Дюплея (рис. 16). Разрезом, окаймляющим наружное отверстие мочеиспускательного канала и продолжающимся на границе слизистого и кожного покрова, выкраивается лоскут, ширина которого должна быть не менее 14-16 см. Края лоскута отсепаровываются от кавернозных тел на 3-4 мм и сшиваются на катетере тонкими синтетическими нитями на протяжении стволовой части. Вторым рядом швов сближают кавернозные тела, третьим - кожу. Для отведения мочи используют уретральный катетер или накладывают цистостому. При этой операции существует опасность образования уретральных свищей по линии совпадения швов уретры и кожи.
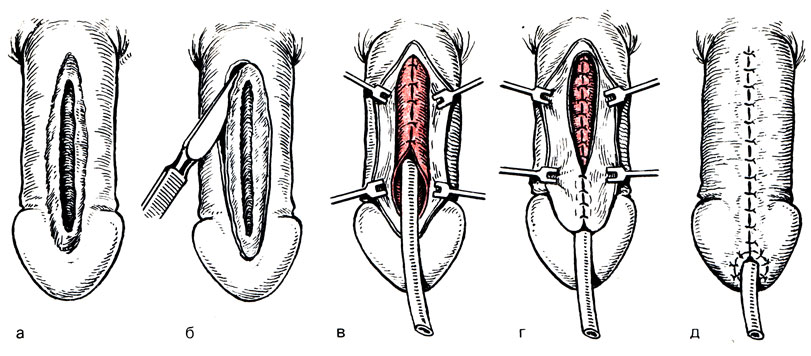
16. Этапы пластики уретры при эписпадии по Дюплею (а - д)
Этого недостатка лишен способ Тирига (рис. 17). При нем линии внутреннего и наружного швов находятся в разных проекциях. Кроме того, за счет мобилизации кожных лоскутов возможно формирование уретральной трубки большого размера. При недостатке кожи рана полового члена может подшиваться к передней брюшной стенке с последующим использованием кожи живота для закрытия кожного дефекта (рис. 18).
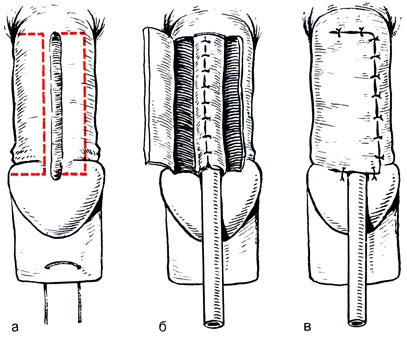
Рис. 17. Пластика уретры при эписпадии по Тиршу (а - в - этапы операции)
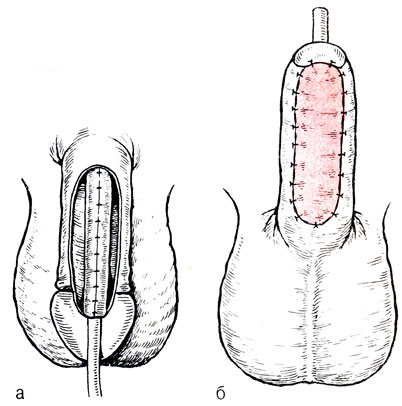
Рис. 18. Закрытие раневого дефекта при пластике уретры по поводу эписпадии (а - б). Пунктиром показана линия разреза кожи живота при вшивании и при отделении полового члена от брюшной стенки
Пластика уретры по Юнгу заключается в перемещении вновь сформированного мочеиспускательного канала на вентральную поверхность полового члена (рис. 19). Разрез производят по обе стороны уретральной борозды и окаймляют наружное отверстие мочеиспускательного канала, который потом мобилизуют до бульбозного отдела. Края лоскута на остальном протяжении полностью отделяют от одного из пещеристых тел и спонгиозного тела головки. С другой стороны лоскут мобилизуют лишь для захвата швами. После формирования уретральной трубки на катетере ее перемещают на вентральную поверхность и фиксируют там за счет сшивания над ней кавернозных и спонгиозных тел. После этого третьим рядом швов сшивают кожу полового члена. Отведение мочи осуществляется с помощью цистостомы.
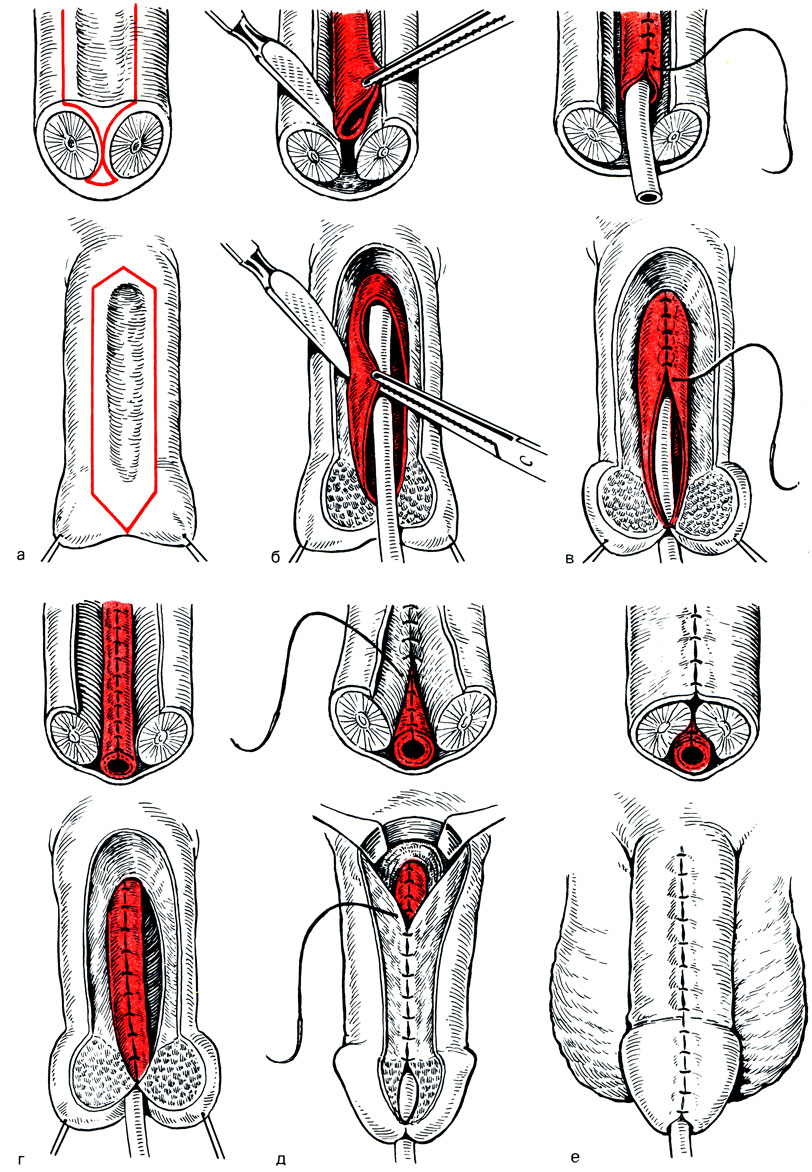
Рис. 19. Этапы пластики уретры при эписпадии по Юнгу (а - е)
У взрослых при пластике уретры нами получены лучшие результаты у оперированных по способу Юнга. Следует отметить, что при всех вариантах операций наиболее трудным моментом является формирование головчатого отдела мочеиспускательного канала.
Скрытый половой член. Считается довольно редко встречающимся пороком развития, при котором половой член не имеет собственной кожи и располагается под кожей лобка, мошонки, промежности или бедра. Эта аномалия должна быть дифференцирована от micropenis или от врожденного отсутствия полового члена, при котором нередко отмечается расщепление мошонки, а наружное отверстие редуцированного мочеиспускательного канала открывается на промежности или в прямой кишке.
Лечение должно быть оперативным и заключается в высвобождении полового члена из клетчатки и формировании собственного кожного покрова.
Для профилактики расстройств психического состояния ребенка, а также для создания благоприятных условий для развития пешеристых тел оперативное лечение показано в возрасте от 3 до 6 лет.
Фимоз, короткая уздечка полового члена. Частым пороком развития полового члена является фимоз - сужение крайней плоти, препятствующее освобождению головки из препуциального мешка. При фимозе внутри препуциального мешка скапливается беловатое сальное вещество (смегма), продуцируемое железами, расположенными на головке полового члена. Смегма может сгущаться, инкрустироваться солями, а при присоединении инфекции - разлагаться, вызывая воспаление головки и крайней плоти полового члена (баланопостит), что в дальнейшем может привести к развитию рака. Выраженный фимоз может вызвать затруднение мочеиспускания у детей, задержку мочи и даже явиться причиной расширения верхних мочевых путей (уретерогидронефроза).
Лечение. У детей нередко удается освободить головку полового члена после расширения отверстия крайней плоти и разъединения рыхлых спаек между головкой и внутренним листком крайней плоти металлическим зондом. У взрослых, а также при выраженном фимозе у детей показана операция - круговое иссечение крайней плоти с последующим сшиванием внутреннего и наружного листков ее, рассечение крайней плоти и др.
Одним из опасных осложнений фимоза является парафимоз, когда вследствие каких-либо причин (половой акт, мастурбация и др.) суженная крайняя плоть сдвигается за головку полового члена, развивается ее отек, что приводит к ущемлению головки и нарушению ее кровоснабжения. При отсутствии срочной помощи может развиться некроз ущемленной головки полового члена.
Лечение парафимоза заключается в попытке вправления обильно смазанной вазелиновым маслом головки полового члена. Если эти попытки не приводят к успеху, то производится рассечение ущемляющего кольца. В последующем показано круговое иссечение крайней плоти в плановом порядке.
Короткая уздечка полового члена может сопутствовать фимозу или встречаться самостоятельно. Короткая уздечка препятствует освобождению головки полового члена из препуциального мешка, вызывает искривление полового члена при эрекции и возникновение боли при половом сношении. При этом короткая уздечка нередко надрывается, вызывая кровотечение.
Лечение заключается в рассечении короткой уздечки в поперечном направлении и сшивании раны продольно.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'