АСКОРБИНОВАЯ КИСЛОТА
Расстановка ударений: АСКОРБИ`НОВАЯ КИСЛОТА`
АСКОРБИНОВАЯ КИСЛОТА (Acidum ascorbinicum; син. витамин C) - органическое соединение, относящееся к витаминам и содержащееся в большинстве растений. Отсутствие его в пище вызывает развитие специфического заболевания - цинги (см.), а недостаточность приводит к развитию гиповитаминоза.
В 1923-1927 гг. Зильва (S. S. Zilva) впервые выделил из лимонного сока вещество с сильным антискорбутным свойством. Он же установил основные свойства этого вещества. В 1930-1933 гг. Тилльманс (J. Tillmans) показал обратимое окисление этого вещества. В 1928-1933 гг. Сент-Дьёрдьи (A. Szent-Györgyi) выделил в кристаллическом виде из надпочечников быка, а также из капусты и паприки вещество, названное им "гексуроновой к-той", получившей затем название "аскорбиновая к-та". Оно оказалось идентичным с антискорбутным веществом Зильвы.
А. к. является производным L-гулоновой к-ты (2-3-эндиол-L-гулоно-1,4-лактон). Наиболее активной формой является L-аскорбиновая к-та. Эмпирическая формула C6H8O6, структурная формула:
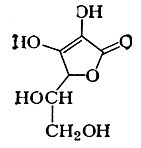
аскорбиновая кислота
Мол. вес А. к. -176,1. Уд. вращение в воде - [α]D20 + 23°; t°пл 192°. Это одноосновная кислота с константой диссоциации pKa -4,25 в воде. В сильно кислой среде А. к. обладает максимумом поглощения при 245 нм, сдвигающимся к 365 нм в нейтральной среде и к 300 нм в щелочной. В чистом виде А. к. представляет собой белые кристаллы кислого вкуса, стойкие в сухом виде и быстро разрушающиеся в водных растворах. 1 г А. к. растворяется в 5 мл воды, 25 мл этилового спирта или 100 мл глицерина. А. к. нерастворима в бензоле, хлороформе, эфире, петролейном эфире и жирах. А. к. реагирует с катионами металлов, образуя аскорбинаты с общей формулой C6H7O6M. А. к. легко окисляется кислородом воздуха. Окисление А. к. ускоряется в нейтральных и щелочных растворах. Оно катализируется светом, ионами меди, железа, серебра и ферментами растений: аскорбиноксидазой и полифенолоксидазой. При окислении А. к. переходит в дегидроаскорбиновую к-ту, обладающую столь же высоким C-витаминным действием, что и А. к. Дегидроаскорбиновая к-та быстро восстанавливается в тканях. Она не содержит конъюгированной системы и не обнаруживает поглощения в ультрафиолете. Наряду с А. к. и дегидроаскорбиновой к-той в растительных продуктах встречается связанная с белком форма А. к. - аскорбиген, - устойчивая к окислению. При необратимом окислении дегидроаскорбиновая к-та после раскрытия лактонового кольца при pH более 4 переходит в 2,3-дикетогулоновую к-ту, а затем в щавелевую и α-треоновую к-ту. Окисление А. к. задерживается тиосульфатом, тиомочевиной, тиоацетатами, флавоноидами, о-дифенолами, метафосфорной к-той, кислыми полисахаридами и др. Большинство белков и аминокислот также задерживает окисление А. к. путем образования комплексов либо с самой А. к., либо с медью. А. к. легко восстанавливает Азотнокислое серебро, растворы брома, йода и 2,6-дихлорфенолин-дофенола. А. к. настолько эффективна в качестве восстановителя, что нашла широкое применение в аналитической химии при определении ряда минеральных элементов и в полярографических исследованиях большого числа веществ, в частности урана и других соединений. А. к. широко распространена в природе (см. таблицу). Она содержится в растениях, гл. обр. в восстановленной форме. Из органов животных богаты А. к. надпочечники, гипофиз, хрусталик, печень. При кулинарной обработке теряется в среднем до 50% А. к. Еще больше теряется при стоянии готовых блюд. Ряд стабилизаторов, находящихся в белке яиц, мясе, печени, крупах, твороге, крахмале, поваренной соли, способствует сохранению А. к. при приготовлении пищи. Длительному сохранению А. к. способствуют: квашение, замораживание, дегидратация, баночное консервирование, варка ягод и фруктов с сахаром (см. также Витаминизация пищевых продуктов).
| Наименование пищевых продуктов | Количество аскорбиновой кислоты |
|---|---|
| Овощи | |
| Баклажаны | 5 |
| Горошек зеленый консервированный | 10 |
| Горошек зеленый свежий | 25 |
| Кабачки | 10 |
| Капуста белокочанная | 40 |
| Капуста квашеная | 20 |
| Капуста цветная | 75 |
| Картофель лежалый | 10 |
| Картофель свежесобранный | 25 |
| Лук зеленый | 27 |
| Морковь | 8 |
| Огурцы | 15 |
| Перец зеленый сладкий | 125 |
| Перец красный | 250 |
| Редис | 50 |
| Редька | 20 |
| Репа | 20 |
| Салат | 15 |
| Томатный сок | 15 |
| Томат-паста | 25 |
| Томаты красные | 35 |
| Хрен | 110-200 |
| Чеснок | Следы |
| Шпинат | 30 |
| Щавель | 60 |
| Фрукты и ягоды | |
| Абрикосы | 10 |
| Апельсины | 50 |
| Арбуз | 7 |
| Бананы | 10 |
| Брусника | 15 |
| Виноград | 4 |
| Вишня | 15 |
| Гранат | 5 |
| Груша | 8 |
| Дыня | 20 |
| Земляника садовая | 60 |
| Клюква | 15 |
| Крыжовник | 40 |
| Лимоны | 50 |
| Малина | 25 |
| Мандарины | 30 |
| Персики | 10 |
| Слива | 8 |
| Смородина красная | 40 |
| Смородина черная | 250 |
| Черника | 5 |
| Шиповник сушеный | До 1500 |
| Яблоки, антоновка | 30 |
| Яблоки северных сортов | 20 |
| Яблоки южных сортов | 5-10 |
| Молочные продукты | |
| Кумыс | 20 |
| Молоко кобылье | 25 |
| Молоко козье | 3 |
| Молоко коровье | 2 |
А. к. получают синтетически из D-глюкозы, восстанавливаемой в D-сорбит, к-рый затем переводится с помощью бактериального синтеза в D-сорбозу, 2-оксо-L-гулоновую к-ту и L-аскорбиновую к-ту. Хорошим стабилизатором А. к. является сульфит натрия, используемый при приготовлении ампульных растворов. Единственным антагонистом А. к. является глюкоаскорбиновая к-та.
Все растения и многие животные синтезируют А. к., за исключением человека, обезьяны, морской свинки, индийской плодовой летучей мыши (Pteropus medius) и краснозадого бульбуля (Pycnonotus cafer Linn.) - птицы из отряда Passeriformes, вследствие отсутствия у них ферментов D-глюкуроноредуктазы и L-гулоно-гамма-лактон-O2-оксидоредуктазы, возможно, из-за врожденного генетического дефекта.
Поступившая в организм человека А. к. всасывается в тонком кишечнике. Общее количество А. к. в организме здорового человека 3-6 г. В плазме крови содержится 0,7-1,2 мг% , в лейкоцитах 20-30 мг% . Ряд оксидаз (аскорбиноксидаза, цитохромоксидаза, пероксидаза, лак- таза и др.) прямо или косвенно катализирует окисление А. к. Синтез А. к. в животном организме происходит из D-глюкуронолактона. Механизм действия А. к. окончательно еще не расшифрован. Она играет важную роль в гидроксилировании пролина в оксипролин коллагена, участвует в окислении аминокислот ароматического ряда (тирозина и фенилаланина), а также в гидроксилировании триптофана в 5-окситриптофан в присутствии ионов меди. А. к. участвует в биогенезе кортикостероидов, оказывает защитное действие на пантотеновую и никотиновую кислоты и способствует ферментативному превращению фолиевой к-ты в фолиновую. У видов, не синтезирующих А. к. (человек, морская свинка), как и у способных к его биосинтезу, А. к. оказывает экономизирующее действие в отношении витаминов B1, B2, A, E, фолиевой к-ты, пантотеновой к-ты, уменьшая расходование, т. е. снижает потребность в них. Этот эффект, по-видимому, связан с редуцирующими и антиоксидатными свойствами А. к.
Суточная потребность человека в А. к. - см. Витамины.
Препараты аскорбиновой кислоты применяют для профилактики и лечения С-витаминной недостаточности, а также при повышенной физиол. потребности организма в А. к. (во время беременности и лактации, при повышенной физической нагрузке, усиленном умственном и эмоциональном напряжении).
В леч. целях А. к. используют в комплексной терапии инфекционных заболеваний и разного вида интоксикаций, при заболеваниях печени, нефропатии беременных, при болезни Аддисона, при вяло заживающих ранах и переломах костей, при заболеваниях жел.-киш. тракта (ахилия, язвенная болезнь и др.), при атеросклерозе. А. к. назначают для профилактики кровотечений при лечении антикоагулянтами.
Назначают А. к. внутрь (после еды), внутримышечно и внутривенно. Леч. дозы для взрослых составляют при приеме внутрь 0,05-0,1 г 3-5 раз в день; парентерально А. к. вводят в виде 5% раствора от 1 до 5 мл. Детям назначают внутрь по 0,05-0,1 г 2-3 раза в день; парентерально 1-2 мл 5% раствора. Сроки лечения зависят от характера и течения заболевания.
При длительном применении высоких доз А. к. следует следить за функцией поджелудочной железы, почек, а также за артериальным давлением, т. к. имеются отдельные наблюдения, свидетельствующие о том, что продолжительный прием значительных количеств А. к. вызывает угнетение инсулярного аппарата поджелудочной железы, способствует развитию почечного диабета и может повышать артериальное давление.
Необходимо соблюдать осторожность при назначении максимальных доз А. к. при внутривенном введении в случаях повышенной свертываемости крови, при тромбофлебитах и склонности к тромбозам.
Формы выпуска: порошок, драже по 0,05 г, таблетки по 0,025 г с глюкозой, таблетки по 0,05 г и по 0,1 г; ампулы, содержащие 1 и 5 мл 5% раствора. Кроме того, А. к. входит в состав различных поливитаминных препаратов.
Сохраняют в хорошо укупоренной таре, предохраняющей от действия света и воздуха.
См. также Шиповник.
Методы определения аскорбиновой к-ты зависят от объекта исследования, концентрации А. к. в объекте, наличия в объекте веществ, мешающих определению, и пр. Объектами исследования могут быть органы и ткани животных, биологические жидкости (кровь, моча и др.), растительные продукты (овощи, фрукты и пр.), готовая пища, медицинские препараты А. к. В перечисленных объектах А. к. находится как в восстановленной, так и в окисленной форме (дегидроаскорбиновая к-та), к-рая может образоваться, напр., при обработке и хранении пищевых продуктов. Поэтому ее также необходимо определять.
Основные этапы определения А. к. следующие: 1) получение материала; 2) хранение полученного материала; 3) экстрагирование А. к. из образца; 4) освобождение полученного экстракта от примесей, мешающих определению А. к.; 5) определение количества А. к.
А. к. легко разрушается, и поэтому обеспечение ее сохранности весьма существенно для любого метода исследования. Разрушение А. к. усиливается под влиянием солнечного освещения, аэрации, повышения температуры и увеличения pH среды. Чем меньше содержание А. к. в анализируемом объекте, тем больше трудностей при ее определении. Нек-рые из методов, напр, определение А. к. в крови и моче, имеют ценность для распознавания степени обеспеченности организма человека А. к. При взятии материала из исследуемого объекта необходимо создать условия для максимального сохранения А. к. в полученной пробе.
Напр., исследуя кровь, нужно взять ее без гемолиза. При необходимости нужно создать такие условия хранения материала, к-рые уменьшают или исключают инактивацию А. к. (холод, добавление консервантов и т. д.). Экстрагирование проводят при pH не менее 4, предварительном связывании ионов металлов, катализирующих окисление А. к., и инактивации ферментов, окисляющих А. к. Для экстрагирования применяют растворы уксусной, трихлоруксусной, щавелевой и метафосфорной кислот. Наиболее предпочтительна 5-6% метафосфорная к-та, хорошо стабилизирующая А. к., осаждающая белки и инактивирующая в сырых растительных объектах фермент аскорбиназу. Освобождение от примесей, мешающих определению, проводят с помощью осаждения последних, а также с использованием различных методов хроматографии (на бумаге тонкослойной, ионообменной).
Для количественного определения содержания А. к. в биологических материалах предложен ряд методов. Так, определение А. к. в моче проводят методом Тилльманса, в основе к-рого лежит способность А. к. восстанавливать нек-рые вещества, в частности 2,6-дихлорфенолиндофенол. Для этого анализируемую пробу титруют 0,001 н. раствором натриевой соли 2,6-дихлорфенолиндофенола до прекращения обесцвечивания окраски раствора. Этот же принцип лежит в основе определения А. к. в плазме крови (см. Фармера-Абт метод). При количественном определении в лейкоцитах применяют метод Бессея (см. Бессея методы). Метод достаточно точен и требует для анализа крайне незначительного количества биологического материала (0,2 мл цельной крови).
При исследовании продуктов, содержащих так наз. редуктоны, к-рые вступают в соединение с 2,6-дихлорфенолиндофенол ом (сиропы, компоты, сушеные овощи, фрукты и др.)" лучше всего применять обработку экстракта формальдегидом [Шиллингер (A. Schillinger), 1966]. При анализе объектов, содержащих естественные пигменты (красители), чаще применяют титрование 2,6-дихлорфенолиндофенолом в присутствии органического растворителя (хлороформа, ксилола, изоамилацетата и др.), экстрагирующих избыток красителя. При определении А. к. в окрашенных фруктовых и ягодных соках применяют амперометрическое титрование. Конечную точку титрования А. к. 2,6-дихлорфенолиндофенолом определяют по изменению потенциала - потенциометрически [Харрис, Марсон (L. J. Harris, L. W. Мarson) и др., 1947] либо по появлению поляризационного тока - амперометрически [Харлампович, Возньяк (Z. Charlampowicz, W. Woznjak) и др., 1969]. Этот метод достаточно точен.
Для определения дегидроаскорбиновой к-ты ее восстанавливают в А. к. с последующим титрованием 2,6-дихлорфенолиндофенолом. Для восстановления применяют сероводород [Тилльманс (J. Tillmans) и др., 1932]. Однако сероводород не полностью восстанавливает дегидроаскорбиновую к-ту. Лучшие результаты получают при ее восстановлении сульфгидрильными соединениями (гомоцистеин, цистеин, 2,3-димеркаптопропанол).
Кроме биологического и окислительно-восстановительных методов определения А, к., используют методы, к-рые основаны на цветных реакциях с А. к. или продуктами ее окисления.
Этими методами проводят определение А. к., дегидроаскорбиновой и дикетогулоновой кислот. Наиболее распространен метод, предложенный в 1948 г. Роу (J. H. Roe) и другими, с применением 2,4-динитрофенил гидразина. Дикетогулоновая к-та, получаемая в ходе анализа при окислении дегидроаскорбиновой к-ты, образует озазоны, имеющие оранжевую окраску. Озазоны растворяют в кислотах (серной, уксусной и смесях соляной и фосфорной кислот) и с помощью фотоколориметрирования измеряют оптическую плотность растворов. Наилучшие условия: температура раствора 37°, время проведения реакции - 6 часов.
Определение А. к. проводится также с использованием меченых изотопов, флюориметрическим методом и др.
А. к. в синтетических препаратах определяется титрованием 0,1 н. раствора йодата калия, 1 мл к-рого эквивалентен 0,0088 г А. к.
Библиогр.: Витамины в питании и профилактика витаминной недостаточности, под ред. В. В. Ефремова, М., 1969; Гигиена питания, под ред. К. С. Петровского, т. 1, с. 89, М., 1971; Покровский А. А. К вопросу о потребностях различных групп населения в энергии и основных пищевых веществах, Вестн. АМН СССР, №10, с. 3, 1966, библиогр.; Modern nutrition in health and disease, ed. by M. G. Wohl a.R. S. Goodhart, p. 346, Philadelphia, 1968; The vitamins, ed. by W. H. Sebrell a. R. S. Harris, v. 1, N. Y.-L., 1967; Wagner A. F. a. Folkers K. A. Vitamins and coenzymes, N. Y., 1964.
Методы определения А. к.- Биохимические методы исследования в клинике, под ред. А. А. Покровского, с. 469, М., 1969; Методическое руководство по определению витаминов A, D, E, B1, B2, B6, PP, C, P и каротина в витаминных препаратах и пищевых продуктах, под ред. Б. А. Лаврова, с. 99, М., 1960; Степанова Е. Н. и Григорьева М. П. Методы определения аскорбиновой кислоты в пищевых продуктах, Вопр. пит., т. 30, № 1, с. 56, 1971; Harris L. J. a. Mapson L. W. Determination of ascorbic acid in presence of interfering substances by "continuousflow" method, Brit. J. Nutr., v. 1, p. 7, 1947; Roe J. H. a. o. The determination of diketo-l-gulonic acid, dehydro-l-ascorbic acid, and 1-ascorbic acid in the same tissue extract by the 2,4-dinitrophenylhydrazine method, J. biol. Chem., v. 174, p. 201,1948; Tillmans J., Hirsch P. a. Siebert F. Das Reduktionsvermogen pflanzlicher Lebensmittel und seine Beziehung zum Vitamin C. Z. Lebensmitt.-Untersuch., Bd 63, S. 21, 1932.
Источники:
- Большая медицинская энциклопедия. Том 2/Главный редактор академик Б. В. Петровский; издательство «Советская энциклопедия»; Москва, 1975.- 608 с. с илл., 8 л. вкл.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'