АНЕМИЯ
Расстановка ударений: АНЕМИ`Я
Содержание
Компенсаторные механизмы при анемии Этиология и патогенез Классификация Патологическая анатомия Клиническая картина Анемия у детей Анемия у беременных Радиоизотопная диагностика Анемия экспериментальная
Анемия (anaemia; греч. отрицательная приставка an- и haima — кровь; син. малокровие) — состояние, характеризующееся уменьшением количества эритроцитов и снижением содержания гемоглобина в единице объема крови. При А. в периферической крови нередко обнаруживаются и качественные изменения эритроцитов — их величины, формы и окраски. При нек-рых А. в крови появляются ядерные предстадии эритроцитов (эритробласты, нормобласты, мегалобласты), незрелые формы эритроцитов (полихроматофилы), эритроциты, содержащие различные включения: цитоплазматические — сидероциты, базофильно- и аурофилъно-пунктированные эритроциты и ядерные — хроматиновые пылинки, кольца Кебота, тельца Жолли (цветн. табл., рис. 1).
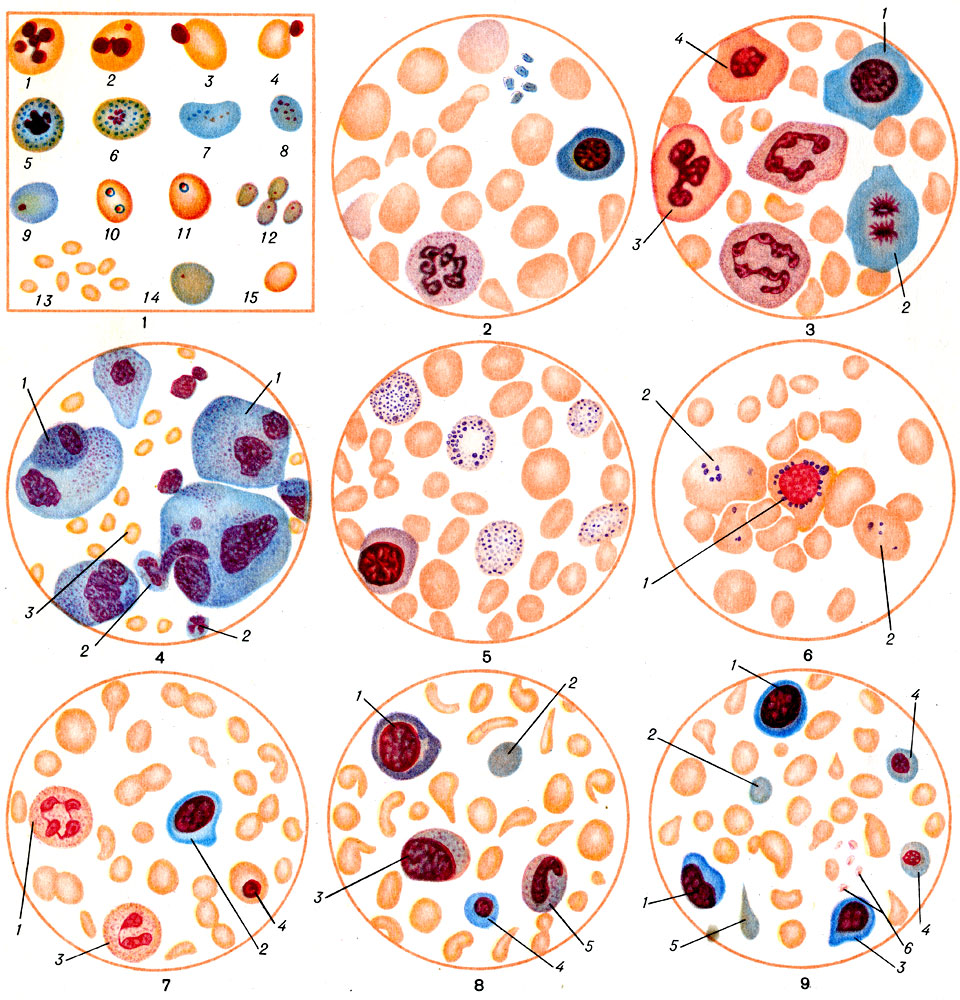
Рис. 1. Различные формы эритроцитов крови при анемических состояниях: 1 и 2 - нормобласты в стадии кариорекеиса; 3 и 4 - энуклеация нормобластов путем выталкивания ядра; 5-9 - распад ядра с образованием телец Жолли в базофильно пунктированных эритроцитах (5 и 6) и полихроматофильных эритроцитах (7-9); 10 и 11-тельца Жолли в ортохромных эритроцитах (после спленэктомии); 12 - хроматиновые пылинки в эритроцитах; 13 - микроциты; 14 - полихроматофильный эритроцит (макроцит); 15 - нормоцит. Рис. 2. Кровь при гиперхромной мегалоцитарной B12(фолиево)-дефицитной анемии (анентеральная спру-анемия). Анизопойкилоцитоз, гиперхромия, полихроматофилия эритроцитов. Рис. 3. Мегалобластическое кроветворение (стернальный пунктат) при анентеральной спру-анемии). Мегалобласты: 1 - полихроматофильный; 2 - в стадии митоза; 3 - оксифильный с "трефовым" ядром; 4 - оксифильный с пикнотическим ядром. Рис. 4. Метастатические раковые клетки (1) в костномозговом пунктате; 2 - нейтрофилы; 3 - эритроциты. Рис. 5. Эритроциты с базофильной пунктацией. Рис. 6. Костный мозг при железо-рефрактерной (сидероахрестической) анемии: 1 - грубозернистый кольцевидный сидеробласт; 2 - грубозернистые сидероциты. Рис. 7. Кровь ребенка при простой гипохромной алиментарной анемии: 1 и 3 - сегментоядерный нейтрофил; 2 - большой лимфоцит; 4 - ортохромный нормобласт. Пойкилоцитоз, анизоцитоз, олигохромемия. Рис. 8. Кровь ребенка при анемии Якша-Гайема: 1 - базофильный мегалобласт; 2 - полихроматофильный эритроцит; 3 - нейтрофильный миелоцит; 4 - полихроматофильный нормобласт; 5 - палочкоядерный нейтрофил. Пойкилоцитоз, анизоцитоз, олигохромемия. Рис. 9. Кровь ребенка при анемии на почве чрезмерного употребления козьего молока: 1 - лимфоцит; 2 - полихроматофильный эритроцит; 3 - базофильный нормобласт; 4 - полихроматофильный нормобласт; 5 - полихроматофильный пойкилоцит (эритроцит); 6 - кровяные пластинки. Пойкилоцитоз, анизоцитоз
От истинной А. следует отличать гемодилюцию, т. е. разжижение крови за счет обильного притока тканевой жидкости, наблюдаемое, напр., у больных в период схождения отеков, после операции с применением искусственного кровообращения. Подобная псевдоанемия проходит по мере того, как исчезает вызвавший ее «отек крови». Истинная А. может маскироваться сгущением крови, напр., при обильной рвоте или профузных поносах; при этом вследствие уменьшения объема плазмы количество эритроцитов в единице объема крови может оказаться нормальным и даже повышенным.
Характерной особенностью истинной А. является либо абсолютное уменьшение массы эритроцитов — эритрона, либо функциональная недостаточность эритрона вследствие уменьшения содержания гемоглобина в каждом отдельном эритроците.
При малокровии в организме нарушаются окислительные процессы и развивается гипоксия (см.). На развитие гипоксии влияет не только степень малокровия, но и быстрота его развития, а также степень и быстрота адаптации организма к изменившимся условиям существования.
Компенсаторные механизмы при анемии
Клиницист нередко наблюдает несоответствие между тяжестью малокровия и активным состоянием больного, что объясняется компенсаторными механизмами, обеспечивающими физиологическую потребность тканей в кислороде.
Основная роль в компенсации анемического состояния принадлежит нервной и сердечно-сосудистой системам: гипоксия приводит к тому, что в кровь поступают недоокисленные продукты обмена веществ. Последние, воздействуя на центральную регуляцию кровообращения, а также на нервно-мышечный аппарат сердца, вызывают учащение сердечного ритма и ускорение кровотока, в результате чего минутный объем крови, выбрасываемой левым желудочком, увеличивается вдвое (до 8 л вместо 4 л в норме). Кроме того, при А. развивается спазм периферических сосудов и в кровеносное русло поступают кровяные резервы из тканевых депо, гл. обр. из подкожной клетчатки. В более легких случаях А. обеспечение тканей достаточным количеством кислорода достигается повышением физиологической активности эритроцитов и проницаемости капиллярной стенки для газов крови. Известное значение в компенсации гипоксии придают железосодержащим энзимам (цитохромоксидаза, каталаза), являющимся потенциальными носителями кислорода, а также процессам бескислородного дыхания при участии глутатиона.
Важнейшая роль в устранении А. и восстановлении нормального состава крови принадлежит костному мозгу, его эритропоэтической функции.
О состоянии эритропоэтической функции костного мозга судят по морфологической картине стернального пунктата (по методу М. И. Аринкина), в частности по количественному соотношению эритро- и лейкобластических элементов; в нормальных условиях это соотношение составляет 1:3 или 1:4. При повышенной регенерации красной крови, когда костный мозг функционирует преимущественно в направлении эритропоэза, соотношение эритро:лейко изменяется в пользу эритробластов, достигая 1:1 или 2:1 и даже 3:1.
В зависимости от преобладания в стернальном пунктате того или иного вида эритробластов различают следующие типы эритропоэза: а) эритробластический, б) пронормобластический, в) нормобластический, г) мегалобластический.
Завершающим этапом эритропоэтической функции костного мозга является процесс поступления зрелых, безъядерных эритроцитов из костного мозга в циркулирующую кровь. Эта важнейшая элиминирующая функция костного мозга выявляется динамическим исследованием основных показателей красной крови — содержания гемоглобина, количества эритроцитов и процента ретикулоцитов.
Этиология и патогенез
А. возникает либо когда убыль эритроцитов в крови (вследствие кровопотери или, кроворазрушения) на данном отрезке времени превышает максимальные возможности регенерации костного мозга, либо вследствие недостаточной эритропоэтической функции костного мозга. Последняя в свою очередь зависит либо от дефицита необходимых для нормального кроветворения веществ (железа, витамина B12, фолиевой к-ты — так наз. дефицитные анемии), либо от неусвоения (неиспользования) данных веществ костным мозгом (так наз. ахрестические анемии).
Патогенез нек-рых А. связан с генетическими особенностями: в одних случаях могут нарушаться энзимные структуры эритроцитов, что приводит к их повышенной чувствительности по отношению к различным внешним агентам (медикаментам, растительным продуктам) с последующим массивным внутрисосудистым гемолизом; в других случаях под влиянием наследственных или приобретенных факторов нарушается синтез тема (см. Гемоглобин), что приводит к состоянию ахрезии, т. е. неиспользованию ряда метаболитов, в первую очередь железа и витаминов кроветворения (витаминов B12, B6, фолиевой к-ты).
Классификация
Разработано множество классификаций А. В соответствии с морфологическим и функциональным состоянием костного мозга, его способностью к регенерации и компенсации анемического состояния различают следующие формы А.: гиперрегенераторную, регенераторную (при острой кровопотере, гемолизе), гипорегенераторную (при хронической кровопотере), пшопластическую, апластическую (при панмиелофтизе), диспластическую или дизэритропоэтическую [при B12-(фолиево)дефицитных состояниях, врожденном многоядерном эритробластозе].
По классификации, предложенной Г. А. Алексеевым, различают три основные группы анемий: А. вследствие кровопотерь — постгеморрагические; А. вследствие нарушенного кровообразования; А. вследствие повышенного кроворазрушения — гемолитические (см. табл. на стр.517). Различают также острую и хрон. А.
Патологическая анатомия
При А. выявляется комплекс изменений, отражающих острую или хрон. недостаточность кровоснабжения. Характер изменений зависит от формы А., фазы развития и проводимой терапии. Макроскопически отмечается бледность и нередко желтушность кожи. При хрон. А. отмечается развитие подкожной жировой клетчатки, жировой ткани в брыжейке, сальнике и вокруг внутренних органов. Мышца сердца дряблая, тусклая, в области папиллярных мышц может наблюдаться желтый крап. Печень на разрезе бледно-серого цвета, рисунок долек стерт. Селезенка часто уменьшена в размерах, капсула морщиниста, на разрезе пульпа дает соскоб. В толще жировой ткани брыжеек могут выявляться множественные мелкие (0,3—0,4 см в диаметре) лимф, узлы темно-красного цвета. Костный мозг плоских костей обычного вида, в средней и нижней трети бедра жировой, с участками кроветворения розово-красного цвета. Иногда костный мозг становится деятельным на всем протяжении бедра. Микроскопическое исследование выявляет жировую дистрофию в мышце сердца и в печени, а также отложение липидов в цитоплазме клеток эндотелия сосудов головного мозга, паренхиматозных органов. Обнаруживаемые в костном мозге изменения различны в зависимости от остроты и формы процесса и эффективности проведенного лечения. Гистологическое исследование биопсий костного мозга позволяет уточнить степень его поражения и способствует дифференциации с другими заболеваниями. Изучение биопсий костного мозга в динамике болезни позволяет установить эффективность терапии и активность процессов регенерации костного мозга.
| Патогенетическая группировка | Основные формы |
|---|---|
| I. Анемии вследствие кровопотерь (постгеморрагические) | а) Острая постгеморрагическая (нормохромная) анемия б) Хроническая постгеморрагическая (гипохромная)анемия |
| II. Анемии вследствие нарушенного кровообразования | |
| А. Железодефицитные анемии | Гипохромные анемии |
| 1. Экзогенная (алиментарная) недостаточность железа | Нутритивная (алиментарная) железодефицитная анемия детского возраста |
| 2. Экзогенная недостаточность железа в связи с повышенными запросами организма | а) Ювенильный хлороз б) Железодефицитная анемия беременных и кормящих женщин в) Инфекционная анемия |
| 3. Резорбционная недостаточность железа (при патологических состояниях желудочно-кишечного тракта), «хирургические» железодефицитные анемии | а) Агастрическая железодефицитная анемия (после резекции желудка) б) Аненторальная железодефицитная анемия (после резекции кишечника) |
| Б. Железорефрактерные (син. сидероахрестические) анемии | а) Наследственная б) Приобретенная |
| В. B12-(фолиево)дефицитные, пернициозные анемии | Мегалобластные гиперхромные анемии |
| 1. Экзогенная недостаточность витамина B12-(фолиевой кислоты) | а) Нутритивная (алиментарная) B12-(фолиево)дефицитная анемия детей при вскармливании козьим молоком, молочным порошком б) Радиационная B12-(фолиево)дефицитная анемия в) Медикаментозная (фенобарбиталовая) B12-(фолиево)дефицитная анемия |
| 2. Эндогенная недостаточность витамина B12-(фолиевой кислоты) вследствие нарушенной ассимиляции пищевого витамина B12; вследствие выпадения секреции желудочного мукопротеина | а) Пернициозная (B12-дефицитная) анемия Аддисона—Бирмера б) Симптоматическая анемия пернициозного (B12-дефицитного) типа при раке, сифилисе, лимфогранулематозе, полипозе желудка, ожогах (коррозивный гастрит), азотемии (экскреторный гастрит) в) Агастрическая анемия пернициозного (B12-дефицитного) типа (гастрэктомия, субтотальная резекция желудка, эзофагоеюно-анастомоз) |
| 3. Нарушенная ассимиляция витамина B12-(фолиевой кислоты) в кишечнике | а) Глистная (дифиллоботриозная) перющиозная B12-(фолиево)дефицитная анемия б) B12-(фолиево)дефицитная спру-анемия, целиакия в) Анентеральная B12-(фолиево) дефицитная анемия (резекция тонкой кишки, дивертикул слепой кишки, терминальный илеит) |
| 4. Повышенное расходование витамина B12-(фолиевой кислоты) | а) Пернициозная B12-(фолиево)дефицитная анемия беременных б) Симптоматическая макроцитарная B12-(фолисво)дефицитная анемия при циррозах печени |
| Г. B12-(фолиево) ахрестические анемии вследствие нарушенной ассимиляции витамина B12-(фолиевой кислоты) костным мозгом | Гиперхромная мегалобластная анемия |
| Д. Дизэритропоэтические анемии, анемии вследствие неэффективного эритропоэза | а) Врожденная (семейно-наследственная) дизэритропоэтическая анемия. Врожденный многоядерный эритробластоз б) Приобретенная дизэритропоэтическая анемия («прелейкозное» состояние) |
| Е. Гипопластические анемии | |
| 1. Воздействие экзогенных факторов (миелотоксическая) | а) Радиационная б) Бензольная в) Медикаментозная |
| 2. Эндогенная аплазия костного мозга | а) Семейная апластическая анемия (Фанкони) б) Детская апластическая анемия (Даймонда—Блекфена) в) Гипоапластическая анемия (Эрлиха) г) Остеопетоозная анемия («мраморная болезнь») |
| Ж. Метапластические анемии вследствие замещения костного мозга | Анемии при лейкозах, миелокарципозах |
| III. Анемии вследствие повышенного кроворазрушения (гемолитические) | |
| А. Анемии, обусловленные экзоэритроцитарными гемолитическими факторами | а) Токсические: при отравлениях гемолитическими ядами (мышьяковистый водород, фосфор, фенилгидразин, сапонины, змеиный яд, грибной яд), при тяжелых ожогах; б) Инфекционные: при малярии, сепсисе (анаэробном, стрептококковом) в) Посттрапсфузионные: вследствие переливания группонесовместимой или резуснесовместимой крови г) Иммунные: изоиммунная гемолитическая болезнь («эритробластоз» плода и новорожденных); аутоиммунные: хроничеолая приобретенная гемолитическая болезнь (Гайема—Видаля), симптоматические — спленогенные при хроническом лимфолейкозе, карциноматозе костного мозга, вирусных инфекциях д) Пароксизмальная холодовая гемоглобинурия е) Механические: в связи с операциями протезирования клапанов и перегородки сердца |
| Б. Анемии, обусловленные эндоэритроцитарными факторами | |
| 1. Эритроцитопатии | а) Врожденные (наследственно-семейные): 1) микросфероцитарная гемолитическая анемия(Минковского—Шоффара); 2) овалоцитарная гемолитическая анемия б) Приобретенная хроническая гемолитическая анемия с постоянной гемосидершгурней и пароксизмальной ночной гемоглобинурией (болезнь Штрюбпнга—Маркиафавы—Микели) |
| 2. Эритроцитоэнзимопении | а) Дефицит глюкозо-6-фосфат-дегицрогеназы: острые гемолитические кризы с гсмоглобинурией, спровоцированные медикаментами, вирусами, растениями (фавизм) б) Дефицит пируваткиназы: врожденная хроническая «несфероцитарная» гемолитическая анемия |
| 3. Гемоглобинопатии | а) β-Талассемии (большая, малая, минимальная) б) α-Талассемия (Н-гемоглобинопатия) в) Дрепаноцитоз (S-гемоглобинопатия, серповидпоклеточиая анемия) г) С-, D-, Е- и другие гемоглобинопатии |
Клиническая картина
Симптомы заболевания бывают более или менее выражены в зависимости от степени анемизации и адаптации больного. Обычно отмечается слабость, быстрая утомляемость, одышка и сердцебиение при физической нагрузке, бледность кожи и слизистых оболочек. При глубокой А., особенно при ее быстром развитии, возникают частые головокружения, шум в ушах, нарушение зрения в виде мелькания «мушек» перед глазами, снижение остроты зрения, иногда вплоть до полного амавроза в связи с нарушением питания зрительных нервов в результате гипоксии. При выслушивании сердца определяется «дующий» систолический шум у верхушки и на соустьях, возникающий в результате гидремии и компенсаторного ускорения кровотока.
Анемия агастрическая возникает обычно после полного удаления (гастрэктомип) или субтотальной резекции желудка. Частичная резекция, широко применяемая при язве желудка, как правило, не сопровождается А. Лишь у части больных (преимущественно у женщин) наблюдается железодефицитная А.
Агастрическая А. бывает железодефицитная и B12-(фолиево)дефицитная; проявляется обычно в сроки от 3 до 5 лет после операции гастрэктомии, иногда раньше — через 1—1/2 года.
От классической пернициозной анемии Аддисона—Бирмера агастрическая B12-дефицитная А. отличается меньшей выраженностью симптомов внутрикостномозгового гемолиза (на почве дизэритропоэза).
Лечение агастрической А. проводится по тем же принципам, что и лечение пернициозной анемии (см.) пли железодефицитной анемии (см.).
Профилактика агастрической А. заключается в своевременном (еще до развития явлений B12-недостаточности) назначении витамина B12 в инъекциях до 100—200 мкг 1—2 раза в месяц, начиная с первых месяцев после операции. Препараты железа применяют по показаниям (при гипохромии эритроцитов, сидеропении).
Анемия анкилостомная вызывается паразитическими червями из класса нематод — анкилостомами (см. Анкилостомидозы). Гризингер (W. Griesinger, 1854) показал, что анкилостомы являются возбудителями так наз. египетского хлороза; «горная анемия», или анемия шахтеров, наблюдавшаяся как массовое заболевание землекопов, работавших при прокладывании Сен-Готардского туннеля, была также анкилостомного происхождения. Патогенез анкилостомной А. связан с потерей крови. Она протекает по типу железодефицитной А. с низким цветным показателем (0,4—0,6), микроцитозом и умеренным ретикулоцито-зом. В тяжелых случаях количество гемоглобина падает до 2—3 г%. Картина белой крови характеризуется лейкопенией и высокой эози-нофилией (до 74%). Диагноз ставят на основании обнаружения яиц анкилостом в фекалиях или дуоденальном содержимом; в последнем можно обнаружить и живые половозрелые особи. Важнейшим лечебным и профилактическим мероприятием является дегельминтизация (см.), при выраженной А. — после предварительного курса антианемического лечения большими дозами железа.
Анемия анентеральная. Под этим названием объединяют различные формы А., связанные с нарушением всасывания в тонкой кишке белков, минералов и витаминов. Наиболее известны пернициозно-анемические состояния, возникающие при затяжных энтеритах, особенно при спру (так наз. пернициозная спру-анемия — цветн. табл., рис. 2 и 3). Пернициозоподобные А. возникают нередко в связи с органическими поражениями кишечника (полипоз, злокачественные опухоли, ретикулосаркоматоз, лимфогранулематоз), при дивертикулах, стриктурах и обширных резекциях тонкой, особенно подвздошной, кишки, при региональных (терминальных) илеитах. Патогенез B12-дефицитной А. в последних случаях связывают с выпадением функции кишечного белка-акцептора. В происхождении этих форм А. имеет значение нарушение всасывания в пораженном кишечнике как железа, так и антианемических факторов — витамина B12, фолиевой к-ты. Имеет значение и дисбактериоз, в результате к-рого нарушаются процессы биосинтеза фолиевой к-ты молочнокислыми бактериями, а размножающаяся в тонкой кишке кишечная палочка конкурирует с макроорганизмом в использовании пищевого витамина B12 и фолиевой к-ты.
Поражения тонкой кишки, сопровождающиеся общей (белковой, минеральной и поливитаминной) недостаточностью, ведут к возникновению смешанной, B12-(фолиево)-железодефицитной, А. Известны также анентеральные железодефицитные А., протекающие по типу хлороза, с низким цветным показателем, низким содержанием железа плазмы, но с макроцитозом эритроцитов.
Лечение анентеральных А. проводят по общим правилам лечения железо-, витамино, B12-(фолиево)дефицитных анемий. Учитывая нарушение кишечной абсорбции, все антианемические препараты следует назначать парентерально.
Анемия ахрестическая (Израэльса—Уилкинсона болезнь) возникает вследствие того, что костный мозг не в состоянии использовать имеющиеся в организме антианемические субстанции. В наст. время рассматривается нек-рыми учеными как эритромиелоз (см.).
Анемия B12-(фолиево)дефицитная. Под этим названием объединяют группу анемических состояний различной этиологии, возникающих в результате недостаточности витамина B12 и (или) фолиевой к-ты, для к-рых характерно, в частности, повышение цветного показателя (1,2—1,8) и появление патологических форм эритроцитов (цветн. табл., рис. 2). См. Пернициозная анемия.
Анемия бензольная — см. Гипопластическая анемия.
Анемия гемолитическая — см. Гемолитическая анемия.
Анемия гипохромная — см. Железодефицитная анемия.
Анемия гиперхромная — см. Пернициозная анемия.
Анемия гипорегенераторная чаще всего возникает как конечная стадия хрон. постгеморрагической А., а также в связи с общей интоксикацией, кахексией и истощением необходимых для построения эритроцитов субстанций — железа, белков, витаминов, микроэлементов. Картина крови при гипорегенераторной А. характеризуется нормо- или гипохромазией, редко гиперхромазией, с выраженными дегенеративными изменениями эритроцитов (анизо- или нойкилоцитоз) при нормальном или незначительно пониженном количестве лейкоцитов (гранулоцитов) и нормальном количестве кровяных пластинок.
Отличие гипорегенераторной А. от собственно гипопластической А. заключается в следующем: 1) как правило, первичным моментом в развитии гипорегенераторной А. является кровотечение, следовательно, патогенетически эта анемия — постгеморрагическая; 2) гипорегенераторная А. никогда не переходит в полную аплазию; 3) костномозговое кроветворение больше соответствует состоянию гипорегенерации (а не гипоплазии); среди эритробластов преобладают базофильные формы; следовательно, имеется не аплазия родоначальных элементов эритропоэза, а истощение фондов железа, белков и витаминов, необходимых для построения зрелых форм красной крови; 4) данное состояние обратимо: длительное и систематическое комплексное лечение выводит костный мозг из торпидного состояния, наступает практическое выздоровление.
Анемия дизэритропоэтическая — см. Дизэритропоэтическая анемия.
Анемия дифиллоботриозная. Этиологическая роль широкого лентеца в развитии А. доказана излечением больных после изгнания паразита, на что впервые обратил внимание С. П. Боткин (1884). Исследование желудочного сока у лиц, инвазированных широким лентецом, показало нормальное содержание внутреннего антианемического фактора. Возникновение А. связывают с нарушением усвоения или разрушением антианемических веществ (витамина B12, фолиевой к-ты). Картина крови в разгар болезни аналогична таковой при пернициозной А. и отличается лишь выраженной эозинофилией (до 30—40%). Костномозговое кроветворение представляет картину мегалобластического эритропоэза. Лечение глистной А. сводится к изгнанию паразита. При истинной дифиллоботриозной А. после дегельминтизации больные быстро выздоравливают без специальной антианемической терапии. При тяжелом течении необходима предшествующая антианемическая терапия (витамин B12), эффект к-рой проявляется еще до изгнания паразита. Профилактика заключается в предупреждении глистных инвазий.
Анемия железодефицитная — см. Железодефицитная анемия.
Анемия железорефрактерная (цветн. табл., рис. 6) — общее название для обширной группы анемических состояний, объединяемых по признаку высокого содержания железа в плазме и рефрактерности к лечению железом, подробнее — см. Железорефрактерная анемия.
Анемия Ледерера — см. Гемолитическая анемия.
Анемия медикаментозная — не столь частое явление, если принять во внимание современные масштабы применения химиотерапевтических средств и антибиотиков. В широком плане различают две группы лекарственных А.
К первой группе относят миелотоксические А., возникающие в связи с цитостатической (химио- или лучевой) терапией, проводимой по поводу опухолевого заболевания или системной патологии крови. Потенциально любое цитостатическое средство, обладающее миелодепрессивным действием, способно вызвать А. гипопластического типа. Ко второй группе относят медикаментозные А., возникновение к-рых связано с индивидуально повышенной чувствительностью организма к определенным лекарственным веществам.
Большинство медикаментозных А. рассматривают либо в плане антивитаминной активности препарата, либо в аспекте аутоиммунной агрессии, где лекарство играет роль гаптена (см. Антигены), либо в аспекте индивидуальной неполноценности энзимных структур эритроцитов, обусловливающей «гемолитическую готовность» в связи с приемом нек-рых медикаментов. При длительном применении массивных доз сульфаниламидов и нек-рых антибиотиков (биомицина, хлорамфеникола, синтомицина, левомицетина) проявляется бактериостатическое действие данных препаратов на микробную флору тонкой кишки; в результате дисбактериоза нарушается биосинтез ряда витаминов, в частности фолиевой к-ты.
Представляют интерес B12-(фолиево) дефицитные А., спровоцированные приемом некоторых противомалярийных, (дараприм) и противоэпилептических средств — дифенина (дифенил-гидантоина, фенитоина), гексамидина (примидона), мезантоина, люминала (фенобарбитала) и других барбитуратов, а также фурадонина (нитрофурантоина) и бутадиена (фенилбутазона). Патогенетическая связь А. с антифолиевой активностью данных препаратов доказывается понижением концентрации фолиевой к-ты в крови лиц, принимавших их, и положительным эффектом лечения фолиевой к-той (в дозах 50—100 мг в день). Менее эффективно лечение витамином B12.
B12-(фолиево)дефицитная А. медикаментозного генеза сопровождается признаками недостаточности витаминов группы В, в частности фолиевой и никотиновой кислот (глоссит, гиперкератоз, понос, изменения психики), чаще развивается у слабых, истощенных больных.
От классической пернициозной анемии Аддисона—Бирмера медикаментозная B12-(фолиево)дефицитная А. отличается сохранностью желудочной секреции, нормальной концентрацией витамина B12 в крови (при нормальной абсорбции меченного по кобальту витамина B12 в кишечнике) и отсутствием неврологических симптомов.
Имеются описания А., возникающей в связи с приемом противотуберкулезных препаратов. Патогенез этой А. сложный; есть основания рассматривать ее как железорефрактерную анемию, обусловленную нарушением синтеза тема в связи с расстройством обмена витамина B6(пиридоксин-пиридоксаль-фосфата).
Лечение медикаментозных А. заключается в прекращении приема препарата, вызвавшего А., и введении фолиевой к-ты.
Анемия медикаментозная гемолитическая (энзимодефицитная) — см. Энзимопеническая анемия.
Анемия миелотоксическая — А. вследствие токсического угнетения костного мозга при различных экзогенных (бензол) и эндогенных (при поражении почек, печени) интоксикациях (см. Гипопластическая анемия).
Анемия мишеневидноклеточная — см. Талассемия.
Анемия пернициозная — см. Пернициозная анемия.
Анемия при почечной недостаточности в большинстве случаев носит гипохромный характер,свойственный железодефицитной А. У нек-рых больных развивается гиперхромная пернициозоподобная А. Отмечается нейтрофильный лейкоцитоз (с сохранением эозинофилов), при уремии до 12000—20000 в 1 мкл. Известную роль в развитии А. при почечной недостаточности играет поражение жел.-киш. тракта. В свете данных об эритропоэтинах (см.) высказывается мнение, что причиной А. при почечной недостаточности является нарушение функции юкстагломерулярного аппарата почек. Согласно другим авторам, установившим тормозящее влияние сыворотки крови почечных больных на пролиферативную активность эритробластов костного мозга, А. при почечной недостаточности возникает под влиянием накопления в крови ингибиторов эритропоэтина. Инактивация ингибиторов эритропоэтина связана с неизвестной еще функцией почек.
Лечение — витаминотерапия, переливание эритроцитной массы. В перспективе — разработка получения эритропоэтинов.
Анемия при поражениях печени. При хрон. диффузных поражениях печени (гепатиты), независимо от этиологии процесса, возникает макроцитарная А. нормохромного или умеренно гиперхромного типа, что связано с нарушением депонирования и утилизации витамина B12, а также фолиевой к-ты. При подострой дистрофии печени макроцитарная А. гиперхромного типа является одним из важнейших показателей тяжелого нарушения функции печени и имеет серьезное прогностическое значение.
Развитие тяжелой пернициозоподобной А. при метастатическом раке печени может служить указанием на первичную локализацию рака в желудке.
При хрон. активных (так наз. люпоидных) гепатитах, циррозах печени, развивающихся по аутоагрессивному механизму, нередко возникает гемолитическая А., протекающая по типу приобретенного аутоиммунного гемолиза, с положительной прямой пробой Кумбса (см. Кумбса реакция).
Анемия при метастазах рака в костный мозг чаще всего развивается при раке предстательной, молочной, щитовидной желез, раке легких, гипернефроме. При метастазировании злокачественной опухоли в костный мозг (миелокарциноз) синдром А. занимает ведущее место в клинической картине заболевания. Исходный очаг процесса (опухоль, давшая метастаз рака в кость) нередко настолько мал, что никакими методами исследования не выявляется. Отличительными особенностями этой А. являются необычайно выраженный эритронормобластоз и лейкемоидная картина крови. Однако в трети случаев, даже при очень значительном распространении метастазов по костям, лейкемоидная реакция может не наблюдаться. Картина крови зависит не только от механического фактора — имплантации в костный мозг раковых клеток, но и от реактивности костного мозга. Между типом опухоли и характером реакции костного мозга не существует видимой связи.
Стернальная пункция (см.) дает возможность диагностировать метастазы в костный мозг даже при отсутствии клинических данных (цветн. табл., рис. 4). Цитологическая диагностика не представляет особых трудностей; наиболее важным признаком раковых клеток является их атипия по сравнению с окружающей миелоидной тканью. Наряду с атипическими, не свойственными костному мозгу клетками, в костномозговом пунктате встречаются неопластические клетки, к-рые в условиях среды костного мозга подвергаются своеобразной метаплазии, приобретая нек-рые свойства миелоидных элементов, в частности азурофильную зернистость. При диффузной метаплазии костного мозга инородной тканью картина крови может приближаться к той, какая наблюдается при хрон. миелолейкозе или остром миелобластном лейкозе (см.).
Анемия свинцовая развивается под влиянием интоксикации организма свинцом (см.) или его соединениями. В наст. время рассматривается как прототип А., связанной с нарушением синтеза тема.
Римингтон (Rimington, 1938) впервые высказал мнение о том, что свинец препятствует вхождению железа в порфириновое кольцо и тем самым нарушает формирование тема из про-топорфирина и железа. Современные исследователи обнаружили в моче больных свинцовой А. значительное содержание δ-аминолевулиновой к-ты (δ-АЛК). Свинец, блокируя ферментные системы, участвующие в синтезе порфиринов, тормозит синтез тема и на более ранней стадии — образование из δ-АЛК порфобилиногена. Как полагают, основная сущность токсического действия свинца заключается в блокировании сульфгидрильных групп ферментов. Непосредственную роль в нарушении синтеза тема играет подавление активности следующих ферментных систем: дегидразы δ-АЛК, декарбоксилазы уропорфириногена, гемсинтетазы. Следствием (не причиной!) неполноценного кроветворения является укорочение жизненного цикла эритроцитов и ускоренный эритролиз, сопровождающийся симптомами квазигемолитической желтухи (гипербилирубинемия, уробилинурия, повышенное содержание стеркобилина в кале).
Клиническая картина свинцовой интоксикации многообразна: симптомы поражения жел.-киш. тракта, нервной и сердечно-сосудистой систем, кроветворных органов. Уже в начальной стадии и при легкой степени свинцовой интоксикации картина крови (цветн. табл., рис. 5) обнаруживает характерные изменения в виде значительного ретикулоцитоза и базофильной пунк-тации эритроцитов. При более выраженной интоксикации развивается А. обычно гипохромного типа, со снижением гемоглобина в тяжелых случаях до 8—6 г%. Наряду с выраженной гипохромией эритроцитов отмечается высокое содержание железа в сыворотке. Костномозговой пунктат характеризуется выраженной эритронормобластической реакцией и сидеробластозом с преобладанием кольцевидных форм.
Диагноз свинцовой интоксикации ставят на основании анамнеза, характерной картины крови (базофильная пунктация эритроцитов и гиперретикулоцитоз, неадекватные степени анемии и гемолиза); окончательно подтверждается обнаружением в моче свинца; особенно большие количества свинца (до 2 мг на 1 л мочи) выделяются после введения комплексона. Известное диагностическое значение, особенно на ранней стадии свинцовой интоксикации, может иметь обнаружение в моче δ-аминолевулиновой к-ты, являющейся наиболее ранним биохимическим признаком нарушенного синтеза тема.
Для лечения в качестве специфического антидота применяют комплексен — динатрийкальциевую соль этилендиаминтетрауксусной к-ты (тетацин-кальций), образующую со свинцом прочный комплекс, легко удаляемый из организма. Препарат вводят в вену в виде 10% раствора по 20 мл ежедневно в течение 5 дней. Обычно проводят 3—4 курса с 4—5-дневными интервалами. Применяют и другие комплексоны: комплецин — внутрь в таблетках (по 2 г через день в течение 20 дней) или в вену (в виде 10% раствора по 20 мл в день в течение 5 дней), Д-пеницилламин (в вену в разовой дозе 1 г).
Разработанная в СССР система диспансерного наблюдения за работниками производств, связанных с добычей, выплавкой или применением свинца, способствует своевременному выявлению легких форм и предупреждению тяжелых форм свинцовой интоксикации.
Анемия серповидноклеточная — см. Серповидноклеточная анемия.
Анемия спленогенная рассматривается в наст. время как первая стадия системного заболевания селезенки, печени и костного мозга, так наз. миело-гепато-лиенального синдрома, или Банти синдрома (см.). Картина периферической крови характеризуется панцитопенией, т. е. количественным уменьшением всех клеточных форм. При этом собственно анемия, т. е. эритроцитопения, не столь выражена; нередко на первый план выступает лейкопения (так наз. селезеночная гиполейкия) или тромбоцитопения, к-рой иногда сопутствует геморрагический диатез (см. Пурпура тромбоцитопеническая). От собственно спленогенной А. следует отличать А., развивающуюся вследствие жел.-киш. кровотечений на почве тромбоза селезеночной вены у больных с тромбофлебитической спленомегалией (см.). При спленогенной А. показана операция удаления селезенки, однако показания к операции должны рассматриваться индивидуально.
Анемия сфероцитарная — см. Гемолитическая анемия.
Анемия тиреопривная развивается на почве гипотиреоза (см.). Различают три вида тиреопривной А.: нормохромную, гипохромную, гиперхромную (пернициозоподобную). Полагают, что дефицит тироксина приводит к расстройству утилизации специфических факторов кроветворения (железа, фолиевой к-ты, витамина B12).
Анемию при зобе Хасимото (см. Хасимото болезнь) рассматривают в наст, время в аспекте аутоиммунного конфликта. В этой связи сочетание гипотиреоза с пернициозной (B12-дефицитной) А. может быть истолковано как результат органоспецифической иммунизации, что доказывается обнаружением антител направленного действия как против клеток щитовидной железы (тиреоглобулина), так и против париетальных клеток фундальных желез (внутреннего фактора Касла).
При А., протекающей на фоне гипотиреоза, наилучший лечебный эффект достигается применением железа и цианокобаламина (витамина B12 в обычной дозировке) в сочетании с тиреоидином (0,1—0,2 г 3 раза в день).
Анемия у детей
В раннем возрасте А. наблюдается очень часто, что объясняется функциональной лабильностью кроветворного аппарата ребенка. Даже незначительные и недлительные погрешности в питании, неблагоприятные условия быта, недостаточное использование свежего воздуха и дневного света, случайные заболевания и т. д. легко вызывают А., причем большое значение имеют индивидуальные особенности ребенка; велика роль наследственности. Нарушенный гемопоэз у детей, особенно в первые годы жизни, приобретает черты эмбрионального типа со склонностью к развитию лейкемоидных реакций. Вместе с тем при устранении причины, вызвавшей А., отмечается выраженная способность кроветворного аппарата к регенерации и восстановлению нормального состава крови.
Алиментарная анемия обычно наблюдается у детей 6—18 мес., получающих однообразную молочную или мучную пищу (цветн. табл., рис. 7).
По клинической картине различают формы легкие, когда общее состояние ребенка почти не нарушено, средней тяжести и тяжелые. При А. средней тяжести отмечается общая пастозность, бледность кожи и слизистых оболочек, увеличение живота, умеренная гиперплазия лимф, узлов и миндалин, запоры. Количество гемоглобина понижается до 8—10 г%, число эритроцитов — до 4000000, редко до 3000000, цветной показатель 0,5—0,7; полихроматофилия, умеренный ретикулоцитоз, единичные нормобласты; число лейкоцитов, лейкоцитарная формула, тромбоциты — в пределах нормы. Сочетание алиментарного фактора с инфекцией значительно ухудшает течение А.
Тяжелая форма А. (алиментарно-инфекционная, анемия Якша—Гайема; цветн. табл., рис. 8) в наст, время почти не встречается. Общее состояние ребенка тяжелое, слизистые оболочки очень бледны, кожа восковидного или желтоватого цвета с кровоизлияниями, почти всегда наблюдается тяжелый рахит, печень и селезенка сильно увеличены; количество гемоглобина и число эритроцитов резко снижены, число лейкоцитов достигает 15—20 тыс., иногда больше, в лейкоцитарной формуле преобладают лимфоциты или нейтрофилы, много ядерных форм эритроцитов и незрелых форм нейтрофильных лейкоцитов.
Иногда алиментарная А. по общей клинической и гематологической картине (цветн. табл., рис. 9) сближается с пернициозной; описывают ее под названием псевдопер-нициозной или алиментарной (нутритивной) мегалобластической А., к-рая развивается на почве однообразного вскармливания козьим молоком или сухими молочными смесями. В патогенезе — недостаточное количество в пище фолиевой к-ты и витамина B12; имеет значение и дефицит витамина C, принимающего участие в образовании из фолиевой к-ты тетрагидрофолиевой; недостаточная продукция гастромукопротеина, нарушение кислотно-щелочного равновесия, аутоинтоксикация в результате усиленных процессов гниения в кишечнике. Дети беспокойны, плохо едят, прибавка в весе недостаточна, слизистые оболочки бледны, кожа с сероватым оттенком; печень и селезенка увеличены. А. нормо-, иногда гиперхромного, реже гипохромыого характера.
Число эритроцитов может уменьшаться до 1000000 и ниже, анизоцитоз, пойкилоцитоз, ядерные формы эритроцитов, ретикулоцнтов мало, базофильная зернистость в эритроцитах, реже — единичные мегалобласты, тельца Жолли, кольца Кебота. Число лейкоцитов несколько снижено или в пределах нормы, наклонность к гиперсегментации нейтрофильных лейкоцитов; число тромбоцитов снижено, нередко снижен также уровень железа сыворотки; в картине миелограммы — усиленный мегалобластический эритропоэз.
Такой же характер А. бывает при целиакии (см.) и других заболеваниях кишечника, когда нарушаются процессы всасывания; относительно часто болеют недоношенные дети (см.).
В лечении главное — рациональное питание с достаточным содержанием белков, витаминов, железа. Показаны препараты с аскорбиновой к-той, способствующей стабилизации легко усвояемого двухвалентного железа, и 1—2% раствором разведенной соляной к-ты, необходимой для ассимиляции пищевого железа. Восстановленное железо дают по 0,1—0,3 г 3—4 раза в день; соли двухвалентного железа (глюконат и аскорбинат железа) — по 0,2—0,5 г 2—3 раза в день, они не уступают по эффективности восстановленному железу и не вызывают у детей диспептических явлений. При затруднениях в приеме порошков и таблеток можно назначать 10% водный раствор лимонно-аммиачного железа по 1 чайы. л. 2—3 раза в день. Хорошее действие оказывает гемостимулин (см.), к-рый применяют по 0,25—0,5 г 3 раза в день. Препараты железа целесообразно назначать в промежутках между приемами пищи. Перед и сразу после приема железа не рекомендуется давать чай, жирные и мучные продукты во избежание образования нерастворимых соединений. При упорных А. более эффективно комбинированное лечение препаратами железа и витамина B12 по 50—100 мкг через день, 10—15 инъекций. При непереносимости приема препаратов перорально и нарушении всасывания может быть применен ферковен по 1—2 мл внутривенно только в стационарных условиях. В резистентных случаях применяют трансфузию зритроцитной массы по 30—75 мл ежедневно 5—7 дней.
Анемия Фанкони — врожденная семейная панцитопения, отчетливо выявляющаяся чаще всего в возрасте 5—7 лет, — см. Гипопластическая анемия.
Семейная гипопластическая анемия Эстрена—Дамешека — см. Гипопластическая анемия.
Анемия Даймонда—Блекфана — см. Гипопластическая анемия.
Пернициозная анемия типа Аддисона—Бирмера у детей наблюдается крайне редко — см. Пернициозная анемия.
В последнее время описано несколько редких форм пернициозопо-добных А., в том числе болезнь Имерслунд (О. Imerslund) — семейная B12-дефицитная А. с сохраненным внутренним фактором Касла и протеинурией, и ювенильная B12-дефицитная А. — следствие функциональной недостаточности желез желудка, вырабатывающих гландулярный мукопротеин при нормальном морфологическом состоянии слизистой оболочки желудка и сохраненной секреции соляной к-ты.
Наследственная мегалобластическая анемия (нарушение метаболизма пиримидинов, в частности оротовой кислоты) описана у двух детей трехмесячного возраста; наследуется, по-видимому, по аутосомно-рецессивному типу. Эта форма А. имеет пернициозоподобный характер с выраженным анизопойкилоцитозом и анизохромией; эритробласты, тельца Жолли, кольца Кебота; нейтропения, умеренная тромбоцитопения; в костном мозге — мегалобластический эритропоэз, сужение гранулоцитарного ростка при наличии гигантских миело- и метамиелоцитов. Оротацидурия. Задержка физического развития. С лечебной целью назначают уридин.
От истинной А. надо отличать кажущуюся, или мнимую, анемию. Дети — практически здоровы и обычно жалоб нет; в периферической крови нормальное содержание гемоглобина и эритроцитов. Бледность кожи у таких детей объясняется особенностями расположения и кровенаполнения кожных капилляров, иногда несколько пониженным артериальным давлением. Эти дети требуют только тщательного соблюдения режима, соответствующего их возрасту.
Анемия у беременных
Беременность — особое физиологическое состояние, сопровождающееся глубокой перестройкой всех видов обмена, к-рая, однако, не обусловливает развития особых форм А., присущих лишь беременным женщинам. Беременность здоровой до этого женщины, по-видимому, не часто провоцирует развитие А. Чаще беременность выявляет латентно протекавший патологический процесс или усугубляет течение существовавшего ранее заболевания. У беременных встречаются обычные клинические формы А., к-рые распространены среди населения вообще.
Следует отличать от истинной А. у беременных иногда сопутствующее беременности состояние гемодилюции — разжижение крови непропорционально возрастающим объемом плазмы, неправильно называемое «псевдоанемией» или «физиологической анемией» беременных. Эдейер (F. L. Adair) и соавт. подсчитали, что объем крови у здоровых женщин за время беременности увеличивается в среднем на 23% (плазмы — на 25%, массы эритроцитов — на 20%). На 16-й нед. беременности обнаруживается нарастающая тенденция к снижению количества эритроцитов и гемоглобина. К 32-й нед. содержание гемоглобина в периферической крови уменьшается на 15% от исходной величины. Показатели допустимой нижней границы гемодилю-ции: гематокрит — 33/67—30/70, гемоглобин — 11 г% и число эритроцитов — 3600000. Гемодилющш клинически не проявляется, причины ее развития не ясны. Определенное значение имеет, вероятно, усиление секреции кортикостероидов, к-рые, несомненно, участвуют в мобилизации жидкости из внутри- и внеклеточных пространств в кровь [М. Г. Колпаков; Блумстедт (Blomstedt)]. Гемодилюция не свойственна здоровым женщинам с неосложненным течением беременности [Хюттен, Пейнтин, Бает, Лунд, Сиссон (Hytten и Paintin; Bast; Lund и Sisson].
Железодефицитная анемия занимает первое место среди А. у беременных. Она обнаруживается у 15—30% беременных, что составляет 75—95% среди больных А. беременных.
По статистике ВОЗ, железодефицитная А. выявляется у 21—80% беременных при исследовании только гемоглобина и у 40—99% при применении более точного диагностического теста — насыщения трансферина. Ведущим фактором в патогенезе является недостаток железа, чаще утилизационного характера. При беременности организму женщины дополнительно требуется 900—1100 мг железа, причем на нужды плода и построение плаценты расходуется от 375 до 500 мг (ВОЗ; Бает). Чем меньше железа поступает в организм беременной извне или резорбируется из жел.-киш. тракта, тем быстрее развивается дефицит. В подобных случаях расходуется депонированное железо. Истощению резервов железа способствуют частые роды, продолжительная лактация, длительные нарушения режима питания, паразитарные заболевания. Несомненно и значение дефицита витамина D, А, С, комплекса В. Угнетению эритропоэза способствует также избыток стероидов, особенно эстрадиола-17β и эстрона.
Беременных с гемоглобином ниже 11 г%, цветным показателем ниже 0,8, числом эритроцитов менее 3600000, гематокритом менее 33/67 и содержанием сывороточного железа ниже 60 мкг% рассматривают как больных железодефицитной А. (ВОЗ). Клиника железодефицитной анемии у беременных проявляется обычными симптомами для этой формы А. (см. Железодефицитная анемия). Значительную .опасность представляют осложнения беременности на фоне А., особенно поздние токсикозы и преждевременная отслойка нормально расположенной плаценты. Полная отслойка плаценты наблюдается в 2,9% случаев, преждевременные роды — в 11,3%, перинатальная детская смертность — от 4,5 до 20,7%.
Пернициозоподобная, B12-(фолиево) дефицитная анемия беременных учащается в декабре — апреле. Средний возраст больных 28—30 лет, преобладают повторнородящие. Заболевание начинается преимущественно во второй половине беременности, реже — в послеродовом периоде. После родов обычно наступает выздоровление, но возможны обострения при последующих беременностях. Заболевание начинается медленно. Иногда присоединяются расстройства жел.-киш. тракта. Отеки, гипертензия и протеинурия часто маскируют истинную природу болезни. В отличие от пернициозной А., тяжелых поражений нервной системы не наблюдается, иногда отмечаются парестезии. Прогноз неблагоприятный как для матери (летальность 4%), так и для плода; преждевременные роды составляют 36%, мертворождаемость — 12% [Гузен (С. J. G. Goosen)].
Дифференциальная диагностика между тяжелой формой железодефицитной и мегалобластной А. основывается на совокупности клинических признаков, картине периферической крови и пунктата костного мозга.
Лечение А. у беременных зависит от характера А. При дефиците железа рекомендуется одновременно назначать препараты, содержащие железо, медь и кобальт (феррокаль, ферробион, ферратол, гемостимулин, феррогематоген, ферковен). При B12-(фолиево) дефицитных анемиях — витамин B12 и фолиевую к-ту.
Следует учитывать и интересы плода, развивающегося в условиях хрон. гипоксии, нарастающего авитаминоза и метаболического ацидоза. Поэтому витамины следует вводить в максимальных дозах, проводить оксигенотерапию и коррекцию кислотно-щелочного равновесия крови. По показаниям — переливания крови. Вопрос о сохранении беременности при А. необходимо решать терапевту и акушеру совместно.
Радиоизотопная диагностика
С помощью радиоактивных изотопов можно определить истинную или ложную А., синтез гемоглобина, величину эритропоэза, скорость и места преимущественного разрушения эритроцитов.
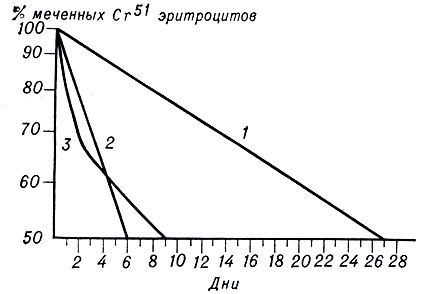
Рис. 1. Продолжительность жизни эритроцитов, меченных Cr51 (в днях): 1 — норма; 2 — врожденная микросфероцитарная гемолитическая анемия; 3 — анемия Маркиафавы—Микели
Основные методики и препараты: определение объема циркулирующих эритроцитов проводится с помощью Cr51, исследование продолжительности жизни эритроцитов — с Cr51 или P32 (диизопропилфлюоро-фосфонатом), места преимущественного разрушения эритроцитов — с Cr51, наличия и величины скрытых кровотечений — с Cr51, интенсивности эритропоэза — с Cr51 или Fe59, всасывания железа — с Fe59 и всасывания витамина B12 — с Co58 (см. Всасывание, радиоизотопное исследование). Большинство тестов проводят in vivo; синтез гемоглобина изучают in vitro.
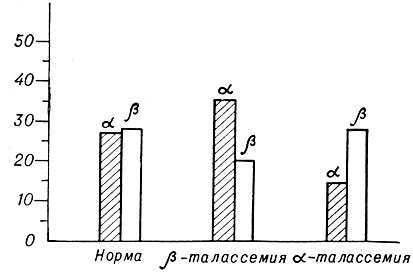
Рис. 2. Включение C14-аспарагиновой кислоты в α- и β-цепи глобина в норме и при α- и β-талаееемии. По оси ординат — импульсы за минуту на микромоль вещества (по Дидковскому)
Индикаторные количества препаратов в зависимости от пробы колеблются от 1—5 мккюри Cr51, Co58, Fe59 до 200 мккюри Cr51. Измерительная аппаратура: счетчики сцинтилляционные жидкостные, а также с цельным и колодезным кристаллами, сканеры и гамма-камеры. Показатели нормы для большинства методов имеют относительное значение, т. к. зависят от деталей применяемых методик.
Информативность радиоизотопных методов больше, чем неизотопных.
В отличие от ранее распространенного метода дифференциальной агглютинации, при к-ром определяется продолжительность жизни только донорских (перелитых) эритроцитов, радиоизотопный метод позволяет определить продолжительность жизни и эритроцитов реципиента. В клинической практике единственным методом, позволяющим определить массу депонированных эритроцитов, является изотопный метод. Радиоизотопный метод более чувствителен, чем неизотопные методы выявления жел.-киш. кровотечений. Он дает возможность количественно определить величину кровопотери на протяжении достаточно долгого времени, что важно в оценке кровопотери как фактора, вызывающего постгеморрагическую А. (см. Желудочно-кишечное кровотечение, радиоизотопная диагностика).
Особенно целесообразно применение радиоизотопных тестов при затруднениях в диагностике таких анемий, как железо- и B12-дефицитные, железорефрактерные, Маркиафавы—Микели (рис. 1), апластическая. Диагноз α-талассемии можно поставить только с помощью радиоизотопного метода. На рис. 2 показано, что в норме включение C14-аспарагиновой к-ты в α- и β-цепи глобина почти одинаково. При β-талассемии уменьшено включение C14-аспарагиновой к-ты в β-цепи, при α-талассемии — в α-цепи.
Радиоизотопное определение степени разрушения эритроцитов в селезенке при гемолитической А. помогает установить показания к спленэктомии.
См. также Кровь, радиоизотопные исследования, Эритроциты, радиоизотопные исследования.
Анемия экспериментальная
С целью изучения механизма возникновения А., процессов регенерации крови, выявления недостаточности кроветворной системы и разработки методов терапии искусственно воспроизводится малокровие у животных.
Экспериментальную А. можно вызвать кровопусканием, разрушением эритроцитов гемолитическими ядами, нарушением целостности различных структурных образований нервной системы, удалением органов и др.
Постгеморрагическую анемию вызывают кровопусканием, к-рое делают однократно в количестве 30 — 40% объема циркулирующей крови (28—35 мл/кг) или повторно 10—15 раз по 10—12%; у кошек можно удалить 40—50% объема крови, у крыс и кроликов — не более 30%. Потеря 60—70% крови смертельна.
Массивное кровопускание вызывает у собак торможение функции коры больших полушарий в течение 7—8 дней, изменение сосудистых и дыхательных рефлексов, понижение артериального давления, гипоксемию и кислородное голодание. Объем крови уменьшается лишь в самом начале кровопотери, затем восстанавливается за счет жидкости, поступающей из тканей. Снижается гемоглобин, число эритроцитов, содержание белков плазмы. Сыворотка животных в течение 5—7 дней приобретает гемолитические свойства: происходит разрушение части эритроцитов и дальнейшее снижение количества эритроцитов и гемоглобина. Эти изменения тем более выражены, чем массивнее кровопускание. Продукты распада эритроцитов способствуют усилению выработки эритропоэтина, стимулирующего эритропоэз. Количество лейкоцитов в течение 4—8 дней увеличивается в основном за счет нейтрофильных со сдвигом влево до юных. Число ретикулоцитов начинает увеличиваться уже через несколько часов и достигает максимальной величины на 5—6-й день, затем постепенно уменьшается. Число тромбоцитов вначале несколько снижается, но быстро восстанавливается и превышает исходный уровень в течение нескольких дней. Эритропоэтическая активность костного мозга усиливается без качественных нарушений кроветворения.
Характер и течение А. зависят от величины кровопотери и регенераторной способности кроветворной ткани.
При многократных кровопусканиях усиление кроветворения может смениться угнетением в связи с истощением кроветворной ткани. После потери 40% объема крови восстановление показателей периферической крови наступает через 20—25 дней.
При повторных кровопотерях восстановление содержания гемоглобина отстает от восстановления количества эритроцитов в связи с истощением запаса железа; соответственно снижается цветной показатель; наблюдается анизо-, пойкилоцитоз, полихромазия эритроцитов, появляются нормобласты в периферической крови. При истощении кроветворной ткани снижается число ретикулоцитов и лейкоцитов. Сроки регенерации зависят от исходного функционального состояния организма и регенераторной способности кроветворной ткани, пола, питания, сезонных колебаний, условий содержания животных в виварии и др.
Гемолитическая анемия вызывается чаще всего введением фенил гидразина, к-рый разрушает старые эритроциты. В то же время продукты распада эритроцитов стимулируют эритропоэз; поэтому восстановление показателей периферической крови происходит быстрее, чем при постгеморрагической А.
2—5% водный раствор фенилгидразина вводят собакам и кроликам под кожу или внутримышечно 4—12 раз с промежутками в 2—3 дня или ежедневно из расчета 0,02—0,04 мг/кг на инъекцию; крысам и мышам вводят однократно внутрибрюшинно из расчета 2—8 мг на 100 г веса.
Степень и быстрота развития А. зависят от дозы фенил гидразина. Под влиянием больших доз количество эритроцитов снижается через 2—3 дня на 40—50%, повышается цветной показатель, появляются в периферической крови полихроматофильные, вакуолизированные и содержащие патологические структуры эритроциты; значительно увеличивается максимальная осмотическая резистентность эритроцитов, повышается число ретикулоцитов; развивается умеренный лейкоцитоз без нарушения лейкоцитарной формулы; увеличивается вязкость и свертываемость крови.
При длительном введении фенил-гидразина появляются мегалоциты и мегалобласты, наблюдается отложение гемосидерина в костном мозге, селезенке и печени. С 8—10-го дня развиваются очаги экстрамедуллярного гемоцоэза, увеличиваются в размере селезенка и печень. В лейкоцитарной формуле — сдвиг влево до миелоцитов. Большие дозы фенил гидразина могут вызвать апластическую А.
Гиперхромная мегалобластическая анемия у животных вызывается внутривенным введением водного раствора сапонина в количестве 1—5 мг/кг в течение 5 дней в возрастающей (по 1 мг в день) дозе. Число эритроцитов уменьшается на 50%, гемоглобина — на 25—30%. Показатели периферической крови восстанавливаются через 20—25 дней. При комбинации сапонина с колларголом (0,3—0,5 мг/кг) А. поддерживается до 40 дней. Аллоксан (180 мг/кг в виде 10% раствора) вызывает А. у животных через 2—3 дня. Как гемолитический яд применяют свинец, толуилендиамин, пирогаллол, мышьяковистый водород, но они вызывают и другие проявления интоксикации.
Нейрогенная анемия может быть вызвана нарушением целостности различных структурных образований нервной системы, напр, денервацией синокаротидной рефлексогенной зоны, селезенки, почек, тонкой кишки и др. А. можно вызвать также повторным введением животным под кожу ацетилхолина, карбохолина и других холинергических веществ. Развивается умеренная гипохромная А. Количество гемоглобина и эритроцитов максимально снижается на 9—15-й день после операции. В крови при этом обнаруживают вещества, угнетающие эритропоэз. Восстановление показателей периферической крови происходит в течение 20—40 дней.
Органопривные анемии развиваются у животных после удаления части или всего желудка, части тонкой кишки или печени, при хрон. потере желчи (через фистулу желчного пузыря), после гипофизэктомии. При сочетании гастрэктомии с нарушением питания у собак развивается гипопластическая А.
Алиментарная анемия. Длительное снижение калорийности пищи, особенно обеднение ее белками, а также недостаток железа, меди, кобальта вызывает у животных А. различного характер а; дефицит фолиевой к-ты и витамина B12 вызывает гиперхромную мегалобластическую А.
Библиогр.: Воспроизведение заболеваний у животных для экспериментально-терапевтических исследований, под ред. Н. В. Лазарева, с. 296, Л., 1954; Гольдберг А. И. Агастрические B12-дефицитные анемии, Томск, 1962, библиогр.; Железодефицитное малокровие и некоторые вопросы регуляции эритропоэза, под ред. С. И. Рябова, Л., 1970; Идельсон Л. И. Нарушения порфиринового обмена в клинике, Л., 1968, библиогр.; Кассирский И. А. и Алексеев Г. А. Клиническая гематология, с. 149, М., 1970, библиогр,; Мосягина Е. Н. Анемии детского возраста, М., 1969, библиогр.; Мухамедзянова Г. С. Гипопластические анемии у детей, М., 1970, библиогр.; Саркисов Д. С. и Ремезов П. И. Воспроизведение болезней человека в эксперименте, с. 84, М., 1960; Фаинштейн Ф. Э. Апластические и гипопластические анемии, М., 1965; Begemann H., Rastetter J. u. Kaboth W. Klinische Hämatologie, Stuttgart, 1970, Bibliogr.; Recent advances in haematology, ed. by A. Goldberg a. M. G. Brain, Edinburgh, 1971, bibliogr.
Патологическая анатомия А. — Абрикосов А. И. Частная патологическая анатомия, в. 1, с. 274, М.—Л., 1947; Давыдовский И. В. Патологическая анатомия и патогенеэ болезней человека, т. 2, М., 1958; Неменова Н. М., Протасова Т. Г. и Воронин В. М. Биопсия костного мозга в диагностике заболеваний системы крови, Арх. патол., т. 33, № 3, с. 3, 1971; Струков А. И. Патологическая анатомия, с. 286, М., 1971; Burkhardt R. Farbatlas der klinischen Histiopathologie, B. u. a., 1970.
Радиоизотопная диагностика А. — Лайта Л. Г. Применение изотопов в гематологии, пер. с англ., М., 1963, библиогр.; Цфасман А. З. Применение радиоактивного хрома в клинике, М., 1964; Radioisotopes in medical diagnosis, ed. by E. H. Belchek a. H. Vetter, L., 1971.
А. беременных — Абдурахманов М. К. Некоторые показатели обмена витаминов B1, B2, B6, C, A, D при нормальной и осложненной железодефицитной гипохромной анемии у беременных, Акуш. и гинек., № 6, с. 10, 1971, библиогр.; Хакимова С. Х. К этиологии и патогенезу железодефицитной анемии у беременных, там же, с. 3, библиогр.; André R. et Najman A. Interprétation des anémies de la grossesse, Sem. Hop. Paris, t. 45, p. 2306, 1965; Bast G. Anämien in der Schwangerschaft, Z. ges. inn. Med., S. 46, 49, 1966, Bibliogr.; Goosen G. J. Anaemias of pregnancy in afr leans, J. Obstet. Gynaec. Brit. Emp., v, 68, p. 994, 1961, bibliogr.; Malinac P. Les frontières de l'anémie &##225;u cours de la grossesse, Concours méd., t. 90, p. 1527, 1968; Nair G. T. R., Agarwal K. N. a. Kotwani B. G. Nutrition deficiency anaemias in later months of pregnancy, J. Obstet. Gynaec. India, v. 20, p. 594, 1970; Rothman D. Folic acid in pregnancy, Amer. J. Obstet. Gynec., v. 108, p. 149, 1970, bibliogr.
Источники:
- Большая медицинская энциклопедия. Том 1/Главный редактор академик Б. В. Петровский; издательство «Советская энциклопедия»; Москва, 1974.- 576 с.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'