АМИДЫ
Расстановка ударений: АМИ`ДЫ
АМИДЫ — производные органических кислот, в которых гидроксильная группа (ОН) замещена аминогруппой (NH2). Играют в организме важную роль в процессах обмена веществ, в частности в биосинтезе белков, процессах обезвреживания аммиака и т. д. Наибольшее значение имеют А. органических кислот, общая формула к-рых RCONH2, где R — радикал (напр., СН3, С2Н5 и т. д.). Простейшими А. карбоновых кислот являются формамид (А. муравьиной к-ты) — НСО⋅NH2, ацетамид (А. уксусной к-ты) — СН3⋅СО⋅NH2. Для живых организмов наибольшее значение имеют мочевина (см.), фосфорный ангидрид карбаминовой к-ты (полуамида угольной к-ты), или карбамоилфосфат, глутамин (см.), аспарагин (см.), глицинамид, А. никотиновой к-ты — витамин РР (см. Никотиновая кислота) и др.
Аспарагин и глутамин входят в число 20 аминокислот, являющихся обычными структурными компонентами белков (см.).
Синтез А. (амидирование кислот) в организмах происходит с затратой энергии высокоэргической связи АТФ (см. Аденозинфосфорные кислоты).
Напр., амидирование аспарагиновой кислоты (см.) можно представить следующей схемой:
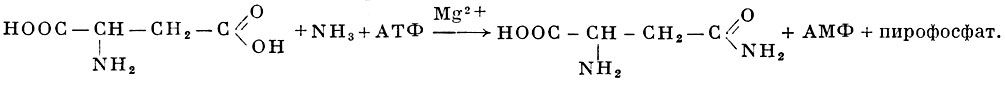
Аналогично происходит п амидирование глутаминовой к-ты. В тканях животных амидирование аспарагиновой к-ты при участии аспарагинсинтетазы может происходить также за счет амидной группы глутамина: аспарагиновая кислота + глутамин + АТФ → аспарагин + глутаминовая кислота + АМФ + пирофосфат. Эта реакция представляет собой одну из десяти известных в наст, время реакций переноса амидной группы глутамина. Амидирование глутаминовой к-ты с использованием амидной группы аспарагина не обнаружено.
Аспарагин и глутамин могут участвовать в реакциях переаминирования (см.) с кетокислотами (см.).
Наиболее важным процессом, в к-ром участвует аспарагин, по-видимому, является биосинтез белков.
В то же время его ближайший гомолог глутамин занимает особое место в обмене азотистых веществ. Это связано с тем, что амидирование глутаминовой к-ты с образованием глутамина служит одним из путей вовлечения аммиака в азотистый обмен (см.). Кроме того, с амидированием глутаминовой к-ты связаны нек-рые специальные функции разных органов, напр. поддержание ионного равновесия (почки, слизистая оболочка желудка), обезвреживание аммиака (мозг).
Большая группа бактериостатических лекарственных веществ, называемых сульфаниламидами, представляет собой производные амидосульфаниловой кислоты (см.). Белки и полиамиды содержат замещенную амидную группу (— NH⋅CO — ).
Библиогр.: Мардашев С. Р. Амиды аминокислот, их обмен и физиологическая роль в животном организме, Усп. совр. биол., т. 40, в. 1, с. 8. 1955; Meister A. Biochemistry of the amino acids, v. 1—2, N. Y., 1965.
Источники:
- Большая медицинская энциклопедия. Том 1/Главный редактор академик Б. В. Петровский; издательство «Советская энциклопедия»; Москва, 1974.- 576 с.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'