АЛЬДОСТЕРОН
Расстановка ударений: АЛЬДОСТЕРО`Н
АЛЬДОСТЕРОН (Aldosteron) — гормон коры надпочечников стероидной природы с минералокортикоидной активностью. А. выделен из надпочечников в кристаллической форме в 1953 г. англо-швейцарской группой исследователей, возглавляемой Симпеоном и Тейтом (S. A. Simpson, J. F. Tait). А. является производным кортикостерона, у к-рого в положении 18 вместо метильной группы находится альдегидная (4-Pregnen-18-al-11,21-diol-3, 20-dion). В растворе А. переходит в 11 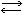 18 циклический полуацеталь (рис. 1).
18 циклический полуацеталь (рис. 1).
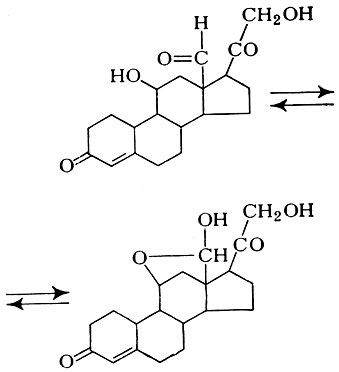
Рис. 1. Структурная формула альдостерона и переход его в полуацеталь
Биосинтез альдостерона и его превращения в организме. А. образуется в клетках клубочковой зоны. Биогенез А. из кортикостерона завершается в митохондриях. Гипотеза Грингарда (P. Greengard, 1967) и соавт. предусматривает несколько этапов с участием энзимов — Е и акцепторов водорода — А (рис. 2). Регуляция секреции А. тесно связана с механизмами водно-солевого гомеостаза и кровообращения. Непосредственными стимулами биогенеза А. является избыток ионов калия, недостаток ионов натрия, ангиотензина 2 и АКТГ. Избыток калия стимулирует биогенез А. Дефицит натрия в организме опосредуется ренин-антпотензионной системой (РАС).
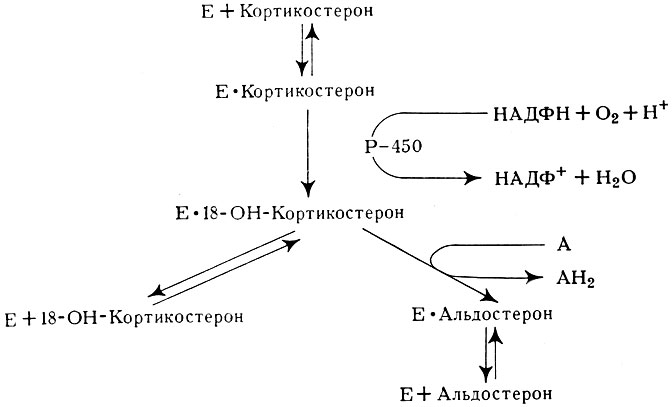
Рис. 2. Схема биогенеза альдостерона из кортикостерона
Синтез и выделение ренина возрастают прежде всего как ответ на раздражение так наз. натриевых рецепторов, локализующихся в гипоталамусе и почках. Почечный натриевый рецептор (macula densa) находится в начальном отделе дистальной порции нефрона. Вторым стимулом для повышения секреции ренина служит раздражение рецепторов приводящей артериолы почки. Оно возникает вследствие уменьшения объема крови и почечного кровотока при кровопотере и снижения минутного объема крови при сердечной недостаточности. Компенсация этих нарушений связана с уменьшением объема сосудистого русла, что служит сигналом для системных рецепторов почки; медиатором стимула для ренин-ангиотензнонной системы могут являться катехоламины. Дефицит натрия действует аналогично кровопотере. На уровне надпочечника дефицит ионов натрия вызывает уникальный эффект, стимулируя биогенез на участке превращения кортикостерона в А. Эта трансформация стероидов зависит от наличия ионов кальция и может ингибироваться посредством 18-ОН-кортикостерона. Ангиотензин 2 усиливает образование эндогенных предшественников ранних этапов биогенеза А.
Преимущественная стимуляция продукции А., возможно, зависит от избирательной рецепции ангиотензина 2 клетками клубочковой зоны надпочечника. Стимулирующий эффект ангиотензина 2 потенцируется совместным действием циклического З1,51-аденозинмонофосфата, избытком ионов калия и недостатком натрия.
Блокада генетической транскрипции в клетках коры надпочечника актиномицином D подавляет стимулирующее действие ангиотензина 2 на продукцию А. АКТГ не определяет регуляцию секреции А. в физиологических условиях. Поддерживая биогенез кортикостероидов в клубочковой зоне, АКТГ повышает ее чувствительность к регуляторным стимулам. В отличие от других кортикостероидов (см.), А. не способен оказывать непосредственное тормозящее воздействие на биогенез по механизму ретроингибирования конечным продуктом. Обратные связи в регуляции секреции А. замыкаются на ренин-ангиотензионной системе.
А. снижает секрецию ренина почкой двумя путями: вызывает угнетение рецепторной функции macula densa и тормозит барорецепторный стимул с приводящих артериол посредством увеличения объема плазмы. Характер ответной реакции надпочечников на регуляторные стимулы зависит в значительной мере от их реактивности. В условиях активации ренин-ангиотензионной системы и адренокортикотропной функции гипофиза надпочечники способны отвечать на действие ангиотензина 2 и АКТГ генерализованной реакцией, выражающейся в повышении продукции А. и кортизола. Ингибиция ренин-ангиотензионной системы нагрузкой натрия снижает альдостеронстимулирующий эффект ангиотензина 2. Реактивность надпочечников по отношению к ангиотензину 2 и АКТГ имеет сезонную периодику.
Период биологической жизни А. составляет 24—36 мин. В плазме крови 50—68% А. связано с белками. Основными метаболитами А. являются тетра-гидро-альдостерон-глюкуронид и 18-оксо-глюкуронид-альдостерон, именуемый кислотнолабильным конъюгатом. К этой же фракции конъюгатов относится и сульфатированный А. Метаболизм А. совершается гл. обр. в печени (85—92%) и в меньшей мере — в почках (5—10%). Тетрагидроконъюгаты образуются только в печени, а кислотнолабильные — в печени и почках. У человека и собаки большинство метаболитов А. экскретируется с мочой (80—90%), однако у крыс большая часть их выделяется с калом и только около 25% с мочой.
Физиологическое действие альдостерона. Биологическая значимость А. заключается в его необычайно высокой способности регулировать обмен натрия и тем самым участвовать в поддержании общего ионного гомеостаза, связанного со многими жизненно важными функциями организма. А. усиливает обратное всасывание натрия в почках, слюнных железах и жел.-киш. тракте. В норме избыток задержанного натрия переводится А. в связанную фракцию в костях и сухожилиях. А. эффективнее дезоксикортикостерона (ДОК) по способности задерживать выведение натрия у адреналэктомированных животных в 25—40 раз и в 100—200 раз — в поддержании соотношения натрий/калий в плазме. Глюкокортикоидная активность А. равняется 1/3 кортизона. Количество А., необходимое для сохранения жизни адреналэктомированных собак, в 10—20 раз меньше количества дезоксикортикостерона и в 500 раз — кортизола. А. по сравнению с кортизолом в большей степени восстанавливает артериальное давление после адреналэктомии. А. потенцирует вазоконстрикторный эффект катехоламинов и оказывает на сердце положительное инотропное действие. Кардиотоннческое действие А. наиболее выражено при гиподинамии сердца, что весьма характерно для адаптивного влияния кортикостероидов. Молекулярные механизмы действия А. реализуются преимущественно посредством генетической индукции синтеза энзимных систем, участвующих в трансмембранном транспорте ионов и митохондриях и в клетке в целом. Это прежде всего энзимы гликолиза и сопряженного окислительного фосфорилированпя и транспортная (Na+ — К+) аденозинтрифосфатаза, обеспечивающая активное выведение натрия из клетки. Возможно, индуцирующее действие А. распространяется также и на пермеазоподобный энзим, вследствие чего может увеличиваться диффузионный поток натрия внутрь клетки.
Для количественной оценки А. в периферической крови используется несколько модификаций метода двойной изотопной метки [Климан, Петерсон (В. Kliman, R. Peterson), 1960]. Сущность метода сводится к процессу превращения А. в альдостерон-диацетат-Н3 в реакции ацетилирования с Н3-уксусным ангидридом. Радиоиммунный метод определения А. в плазме периферической крови [Бейярд (F. Bayard) с соавт., 1970] основывается на измерении конкурентного взаимодействия А. испытуемой плазмы и меченого стандарта гормона с антителами к альдостерону. Антитела вырабатываются после введения кроликам А., ковалентно связанного с кроличьим сывороточным альбумином.
Для определения А. в крови, оттекающей от надпочечников, или конъюгатов А. в моче используются различные варианты бумажной и тонкослойной хроматографии с последующей количественной оценкой по реакции с тетразоловым синим.
Количество А., образуемое надпочечниками здоровых людей, чрезвычайно мало по сравнению с другими кортикостероидами — всего 75—300 мкг за 24 часа. У человека в покое при горизонтальном положении тела секреция А. равняется 24 нг/мин, а концентрация в плазме периферической крови — 2—17 нг%; суточная экскреция тетра-гидро-альдостерон-глюкуронида в норме равняется 15—80 мкг, кислотнолабильных конъюгатов — 3—16 мкг и свободного А. — 0,05—0,30 мкг. Секреция А. имеет четко выраженный суточный ритм с максимумом в дневные часы, если человек утром переходит в вертикальное положение. Медиатором постуральной регуляции секреции А. служит ренин-ангиотензионная система. Секреция А. возрастает при беременности, малом содержании натрия или избытке калия в пище, при кровопотере, сердечной недостаточности, почечной гипертонии, циррозе печени, гидропексическом синдроме и др. (см. Гидропексический синдром, Гиперальдостеронизм).
Препараты с минералокортикоидной активностью могут применяться в клинике с терапевтической целью при аддисоновой болезни, острой надпочечниковой недостаточности, ортостатических циркуляторных расстройствах, шоке, кровопотере и токсемии с явлениями гиподинамии сердца (см. Дезоксикортикостерон). Ингибиторами А. являются спиронолактоны (альдактон, верошпирон и др.).
См. также Надпочечники.
Библиогр.: Альдостерон и адаптация к изменениям водно-солевого режима, под ред. М. Г. Колпакова, Л., 1968; Машковский М. Д. Лекарственные средства, ч. 1, с. 392, М., 1972; Сергеев П. В., Сейфулла Р. Д. и Майский А. И. Молекулярные аспекты действия стероидных гормонов, М., 1971, библиогр.; Стероидные гормоны, под ред. Н. А. Юдаева, М., 1969; Functions of the adrenal cortex, ed. by K. W. Me Kerns, v. 1, N. Y., 1967; Glaz E. a. Vecsei P. Aldosterone, N. Y., 1971, bibliogr.
Источники:
- Большая медицинская энциклопедия. Том 1/Главный редактор академик Б. В. Петровский; издательство «Советская энциклопедия»; Москва, 1974.- 576 с.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'