АДЕНОЗИНФОСФОРНЫЕ КИСЛОТЫ
Расстановка ударений: АДЕНОЗИНФО`СФОРНЫЕ КИСЛО`ТЫ
АДЕНОЗИНФОСФОРНЫЕ КИСЛОТЫ (адениловые нуклеотиды) — биологически активные вещества, представляющие собой фосфорные эфиры аденозина. Среди А. к. различают монофосфорные производные аденозина: аденозинмонофосфорные, или адениловые, кислоты (АМФ) и полифосфорные производные (аденозиндифосфорная — АДФ и аденозинтрифосфорная — АТФ) кислоты, а также производные, содержащие еще большее число остатков фосфорной к-ты, среди к-рых описаны аденозинтетрафосфорная и аденозинпентафосфорная кислоты. При полном гидролизе А. к. дают аденин (см. Пуриновые основания), рибозу (см.) и фосфорную к-ту. При неполном гидролизе можно получить аденозин и соответствующие рибозофосфорные кислоты. Остаток фосфорной к-ты в адениловых кислотах соединен сложноэфирной связью с гидроксилом рибозы в положении 5′, 3′ или 2′. Все эти три изомера аденозин-монофосфорных кислот встречаются в природе. При гидролизе нуклеиновых кислот (см.) получаются аденозин-3′-монофосфорная и аденозин-2′-монофосфорная кислоты («дрожжевые адениловые кислоты»).
В свободном виде преимущественно встречается аденозин-5′-монофосфорная к-та, впервые полученная Эмбденом (G. Embden) в 1927 г. из мышц кролика и иногда называемая «мышечной» адениловой к-той:
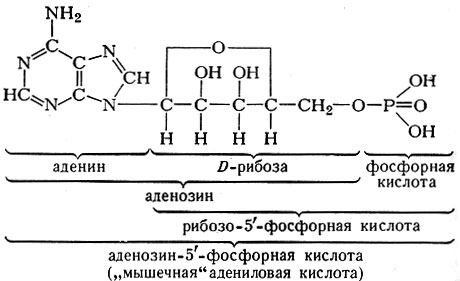
Из различных тканей выделены также аденозин-2′, 3′- и аденозин-3′, 5′-циклофосфаты, т. е. циклические АМФ, в к-рых остаток фосфорной к-ты образует эфиры соответственно с гид-роксилами у второго и третьего или третьего и пятого атомов остатка рибозы. Циклическая 3′, 5′-АМФ играет важную биологическую роль, напр, выполняя функцию активатора фосфорилазы (см.) и других ферментов.
Аденозинполифосфорные кислоты обычно являются производными 5′-АМФ. В тканях организмов содержатся также дезоксиаденозинфосфорные кислоты, в к-рых D-рибоза заменена на D-дезоксирибозу.
Дезоксиаденозинфосфорные кислоты присутствуют в организме в свободном виде, их получают также и при гидролизе дезоксирибонуклеиновых кислот (см.). Все А. к. являются сильными кислотами и в природе находятся в виде солей. А. к. интенсивно поглощают ультрафиолетовое излучение в области ок. 260 нм, они являются сильными комплексообразователями и в природе часто находятся в виде комплексной соли с магнием. Свободные А. к., а также их щелочные и щелочноземельные соли легко растворимы в воде. Соли тяжелых металлов образуют нерастворимые осадки.
Аденозин—9-β-В-рибофуранозиладенин. Представляет собой соединение аденина и D-рибозы. Последняя своим первым углеродным атомом присоединена β-гликозидной связью к девятому атому аденина. Мол. вес 267,24, t°пл 229°, оптически активен [α]D — — 60°. Хорошо растворим в горячей воде, плохо в холодной. Под действием кислот гидролизуется на аденин и рибозу. При ферментативном дезаминировании (см.) в организме превращается в инозин с последующим образованием мочевой к-ты, являющейся конечным продуктом пуринового обмена.
Аденозин-5′-моддофосфорыая кислота. Хорошо растворима в горячей воде. Плавится при t° 198 — 200° с разложением, [α] D = — 47,5° (в 2% едком натре), при щелочном гидролизе отщепляет фосфорную к-ту и образует аденозин. При ферментативном или химическом дезаминировании этого соединения образуется инозиновая кислота (см.).
Аденозин-3′-монофосфорная кислота. Образуется при щелочном гидролизе рибонуклеиновых кислот, плавится с разложением при t° 208°, [α] D в воде = —38,5°. При кислом гидролизе расщепляется на аденин и фосфорибозу. В отличие от аденозин-5′-фосфорной («мышечной» адениловой) к-ты, не дезаминируется мышечной дезаминазой адениловой к-ты и не фосфорилируется с образованием полифосфорных производных.
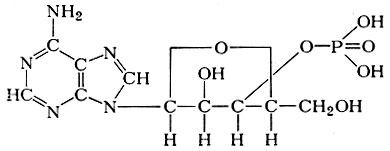
Аденозин-3′-фосфорная кислота («дрожжевая адениловая кислота»)
Аденозин-2′-монофосфорная кислота и аденозин-2′, 3′-циклическая монофосфорная кислота. Образуются при щелочном гидролизе рибонуклеиновых кислот и физиологического значения, по-видимому, не имеют.
Аденозинмонофосфорные кислоты являются наряду с другими нуклеотидами важнейшей составной частью нуклеиновых кислот (см.) и встречаются как в их составе, так и в свободном виде во всех тканях живых организмов. А. к., находящиеся в начале полинуклеотидной цепи м-РНК, имеют значение для инициации биосинтеза белков (см. Белки). Конечный остаток аденозина в транспортных РНК существен для связывания их с рибосомами. В составе РНК содержатся последовательности, состоящие только из адениловых нуклеотидов, а в клетках образуется полинуклеотид, состоящий только из остатков адениловой к-ты. Физиологическая роль этого полинуклеотида до сих пор не ясна. 5'-АМФ является важным компонентом адениловой системы (см. ниже) и принимает участие во многих биологически важных реакциях.
Особую роль играет аденозин-3′, 5′-циклофосфат (циклическая АМФ);
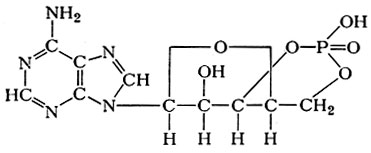
Аденозин-3′, 5′-циклофоефат
Этот нуклеотид является медиатором целого ряда гормонов и участвует в регуляции многих биохимических реакций в клетках. Циклическая 3Аденозин-3′, 5′-циклофоефат, 5Аденозин-3′, 5′-циклофоефат-АМФ (цАМФ) образуется в клетках под действием фермента аденилатциклазы. Этот фермент катализирует реакцию:
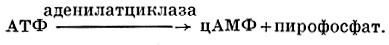
Другой фермент (цАМФ диэстераза) осуществляет расщепление фосфоэфирной связи цАМФ у третьего углеродного атома рибозного остатка с превращением цАМФ в 5′-АМФ. Многие гормоны (глюкагон, адреналин и норадреналин, простагландины, ряд гормонов гипофиза и др.) активируют аденилатциклазу, осуществляя свое действие с помощью образующейся цАМФ. Так, напр., цАМФ, образующаяся при активации аденилатциклазы глюкагоном или адреналином, превращает неактивную киназу фосфорилазы в активную форму. Последняя осуществляет реакцию фосфорилирования (см.) неактивной фосфорилазы b с образованием активной ее формы (фосфорилазы а), участвующей в распаде гликогена (см.). Показано также участие цАМФ и в активации ряда других ферментов в качестве медиатора действия гормонов. Имеются указания, что и в других реакциях действие цАМФ состоит в активации протеинокиназ. Предполагают, что такой же механизм лежит в основе стимулирующего действия цАМФ на биосинтез белков, катаболизм липидов, образование стероидов и проницаемость биологических мембран. Аденилатциклаза обнаруживается гл. обр. в различных клеточных мембранах. В связи с этим высказывалось предположение, что, действуя на комплекс АТФ с кальцием в мембранах, этот фермент наряду с образованием цАМФ приводит к освобождению ионов кальция, к-рые влияют на состояние мембран (см. Мембраны биологические).
Аденазиндифосфорная кислота (аденозинпирофосфорная кислота, аденозиндифосфат, АДФ). Представляет собой фосфоангидрид 5′-АМФ. Конечный остаток фосфорной к-ты в АДФ соединен с АМФ высокоэргической связью. Он отщепляется от АДФ в процессе гидролиза 1н. НС1 при t° 100° за 7 мин. АДФ обратимо превращается в АТФ и в 5′-АМФ, образуя вместе с ними так наз. адениловую систему, играющую важнейшую роль в целом ряде процессов обмена веществ и энергии (см.).
Аденозинтрифосфорная кислота (аденозинтрифосфат, аденилпирофосфорная кислота, АТФ) была впервые получена Ломанном (К. Lohmann) в 1929 г. из мышц лягушки. АТФ представляет собой пирофосфорный ангидрид 5′-АМФ, она является сильной четырехосновной кислотой, легко растворимой в воде. АТФ содержит два высокоэргичееких остатка фосфорной к-ты (соответствующие связи на рисунке обозначены волнистой чертой). АТФ вместе с другими нуклеозидтрифосфатами является субстратом для синтеза рибонуклеиновых кислот в РНК-полимеразной реакции. АТФ является универсальным, богатым энергией (высокоэргическим) соединением (см. Высокоэргические соединения, Биоэнергетика).
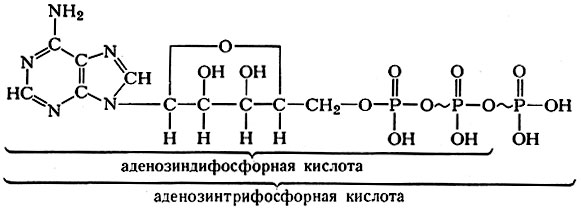
АТФ образуется из АДФ путем фосфорилирования за счет энергии, освобождающейся при окислении органических веществ. АТФ вместе с АДФ и с 5′-АМФ образуют адениловую систему. В норме в мышцах и в других тканях АТФ составляет ок. 75% адениловых нуклеотидов, на долю к-рых в свою очередь приходится ок. 87% общего фонда свободных нуклеотидов. Энергия, накопленная в виде АТФ, используется в огромном числе различных эндергонических процессов, т. е. требующих затрат энергии. К их числу относятся различные формы движения, включая мышечное сокращение, внутриклеточный транспорт ионов и других веществ, биосинтез белков, нуклеиновых кислот, фотосинтез и т. д. Все эти реакции катализируются специфическими ферментами, переносящими на другие вещества остаток ортофосфорной, пирофосфорной или адениловой кислот. Под действием ферментов аденозинтприфосфатаз (см.) АТФ отщепляет остаток фосфорной или пирофосфорной к-ты. В качестве примера реакций с участием АТФ, в к-рых переносится остаток ортофосфорной к-ты, можно привести образование глюкозо-6-фосфата под действием гексокиназы в присутствии ионов магния:
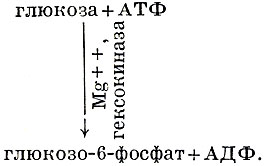
В ряде реакций, напр, при образовании 5-фосфо-α-В-рибозилпирофосфата (ФРПФ) в реакции, катализируемой ферментом АТФ (D-рибозо-5-фосфат - пирофосфотрансферазой), с АТФ переносится пирофосфат с освобождением АМФ:
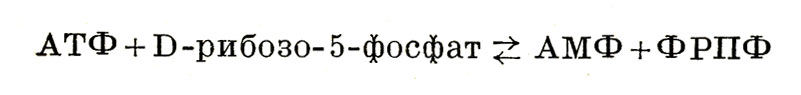
Наконец, группа реакций связана с переносом остатка АМФ и освобождением пирофосфата. К этим реакциям относятся образование аминоациладенилатов (промежуточного продукта синтеза белков):
АТФ + аминокислота → аминоациладенилат + пирофосфат
при участии фермента аминоациладенилатсинтетазы, синтез коферментов, содержащих остатки АМФ, как, напр., никотинамидадениндинуклеотида (НАД) или флавинадениндинуклеотида (ФАД) и др. Остатки адениловых кислот входят в состав многих коферментов и других биологически важных веществ, среди к-рых можно назвать вышеупомянутые НАД, ФАД, НАДФ, а также кофермент А, аденозилметионин, аденилилсулъфат и др. В тканях организмов обнаружены также аденозинтетрафосфат, содержащий четыре остатка фосфорной к-ты, и аденозинпентафосфат, содержащий пять остатков фосфорной к-ты. Однако эти соединения не заменяют АТФ, и биологическая роль их остается неясной.
АТФ, АМФ, АДФ, а также аденозин обладают выраженной фармакодинамической активностью: понижают кровяное давление, активируют мускулатуру матки и других органов, благодаря чему они находят применение при спазмах сосудов, миокардиодистрофии, мышечной дистрофии (см. Аденозинтрифосфорная кислота, Мышечноадениловый препарат).
Библиогр.: Диксон М. и Уэбб Э. Ферменты, пер. с англ., М., 1966; Микельсон А. М. Химия нуклеозидов и нуклеотидов, пер. с англ., М., 1966; Химия и биохимия нуклеиновых кислот, под ред. И. Б. Збарского и С. С. Дебова, Л., 1968; Jost J.-P. a. Rickenberg H. V. Cyclic AMP, Ann. Rev. Biochem., v. 40, p. 741, 1971, bibliogr.; Mandel P. Free nucleqtides in animal tissues, Progr. Nucleic Acid. Res., v. 3, p. 299, 1964, bibliogr.; Rоbisоn G. A., Butcher R. W. a. Sutherland E. W. Cyclic AMP, Ann. Rev. Biochem., v. 37, p. 149, 1968, bibliogr.
Источники:
- Большая медицинская энциклопедия. Том 1/Главный редактор академик Б. В. Петровский; издательство «Советская энциклопедия»; Москва, 1974.- 576 с.
|
ПОИСК:
|
© Анна Козлова подборка материалов; Алексей Злыгостев оформление, разработка ПО 2001–2019
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://sohmet.ru/ 'Sohmet.ru: Библиотека по медицине'